Цель урока – дать понятие о многоатомных спиртах, развить понятия о взаимном влиянии атомов, зависимости применения от свойств веществ; провести исследование- обнаружение многоатомных спиртов в жевательной резинке.
Задачи:
- обучающие – формирование представлений о многоатомных спиртах (отличие их от одноатомных), ознакомление с физическими и химическими свойствами многоатомных спиртов, их распознаванием и применением;
- развивающие–способствовать формированию познавательной активности учащихся на уроке, с использованием интерактивной SMART-доски, мультимедийных презентаций, демонстрационных, исследовательских опытов;
- воспитывающие – создать условия для развития способности использования знаний для принятия обоснованного решения.
Тип урока: урок изучения нового материала
Методы обучения:
- организация и осуществление учебно-познавательной деятельности:
- перцептивныеметоды – словесные (лекция учителя), наглядные (SMART-презентаций), практические (демонстрация опытов);
- логические методы – аналитические;
- гностические методы – исследовательские (исследование состава жевательных резинок);
- управление учением – работа под руководством учителя; самостоятельная работа обучающихся: с книгой, письменная работа в тетрадях;
- стимулирование и мотивация учения:
- стимулирование интереса к учению - учебная дискуссия, занимательность;
- стимулирования долга и ответственности к учению - убеждение в значимости учения, поощрение в учении;
- контроль и самоконтроль в обучении:
- устный контроль – индивидуальный, фронтальный опрос.
Форма проведения урока: исследовательский, мультимедия- урок
Дидактические средства:
- учебник под редакцией О.С.Габриеляна «Химия 10 класс»;
- интерактивная SMART-Board доска;
- программа Notebook;
- компьютер;
- проектор;
- SMART- презентация «Многоатомные спирты» (Приложение 4);
- раздаточный материал по строению и физическим свойствам многоатомных спиртов (SMART-слайды № 8,12) (Приложение 5);
- реактивы для демонстрации опытов учителю: глицерин, этиленгликоль, растворы гидроксида калия, сульфата меди (II), вода дистил., химические стаканы;
- реактивы для проведения исследования учащимися: жевательные резинки, растворы гидроксида калия, сульфата меди (II), вода дистил., химические стаканы;
- демонстрационный материал:
- образцы косметических средств: мыло, крем для рук, помада, гель для душа, крем для лица, краска для волос, зубные пасты;
- образцы жевательных резинок (различные).
Методическая литература: Габриелян О.С. Химия.10 класс: Настольная книга учителя /О.С.Габриелян. И.Г.Остроумов/. - М.: Дрофа, 2004.-480с.
План урока:
1. Организационный момент.
На рабочих столах учащихся подготовлены:
- Листы, с тремя вариантами заданий для контроля.
- Ящики с реактивами: жевательные резинки, растворы гидроксида калия, сульфата меди (II), вода дистил., два химических стакана.
- Образцы косметических средств.
- Раздаточный материал по строению и физическим свойствам многоатомных спиртов (SMART- слайды № 9,13).
Вступительное слово учителя.
Подготовка к проведению химического исследования «Обнаружение многоатомных спиртов в жевательных резинках».
Повторение классификации, изомерии, химических свойств одноатомных спиртов:
- В-1: индивидуальный контроль знаний учащихся с выбором заданий: тестовый контроль –«4» (Приложение 1), составление самими учащимися заданий для контроля - «5»; составление уравнений реакций одноатомных спиртов – «5» (Приложение 2);
- В-2: фронтальный контроль по слайдам SMART-презентации.
2. Изучение новой темы.
Строение, физические свойства и применение многоатомных спиртов.
Демонстрация растворимости глицерина.
Химические свойства многоатомных спиртов.
Демонстрация качественной реакции многоатомных спиртов.
Исследование содержания многоатомных спиртов в жевательной резинке.
3. Подведение итогов урока. Вывод.
4. Домашнее задание.
5. Закрепление учебного материала (тестовый контроль).
Ход урока
1. Организационный момент.
1.1. Вступительное слово учителя.
Давайте, почитаем, этикетки на упаковках изделий, которых я просила вас принести на этот урок: крема, мыла, кондитерские изделия, зубные пасты, жевательные резинки. (SMART-слайд № 2). Очень часто встречаются названия: глицерин, пропиленгликоль, сорбит, ксилит, маннит - это и есть многоатомные спирты.
Я предлагаю вам такой план урока (SMART-слайды № 3,4).
Но прежде проведём подготовительную часть эксперимента.
1.2. Подготовка к проведению химического исследования «Обнаружение многоатомных спиртов в жевательных резинках» ( SMART-слайд № 5).
Опыт 1. В химический стакан положите пластинку жевательной резинки и прилейте небольшое количество дистиллированной воды. Настаивать 15-20 минут.
1.3. Повторение классификации, изомерии, химических свойств одноатомных спиртов.
Для проведения повторения класс делится на «Вариант - 1» и «Вариант - 2». На этом уроке для обучающиеся под «1- вариантом» проводится индивидуальный контроль знаний с выбором заданий:
- тестовый контроль (два варианта заданий)– отметка «4» (Приложение 1);
- работа с дидактическими карточками - составление уравнений реакций одноатомных спиртов – отметка «5» (Приложение 2);
- составление самими учащимися заданий для контроля –«5» (Приложение 3).
Для обучающихся под «2-м вариантом» - фронтальный контроль по слайдам SMART-презентации (SMART-слайды № 7,8,9) (Приложение 4)
2. Изучение новой темы.
2.1. Строение и физические свойства многоатомных спиртов.
Ознакомление со строением и свойствами некоторых представителей многоатомных спиртов (SMART- слайды № 10-14). Чтобы сэкономить время урока, материалы SMART-слайдов № 10-14 распечатывают каждому обучающемуся, и они их прикрепляют в свои тетради.
2.2. Демонстрация растворимости глицерина.
Демонстрационный опыт: вода + глицерин → перемешать.
Вывод: хорошо растворим в воде.
Сравнивают физические свойства одноатомных и многоатомных спиртов ( SMART-слайд № 16). Выявляем причину такого различия (причина – число гидроксогрупп) (SMART-слайд № 17).
В молекуле глицерина имеются 3 гидроксогруппы, значит число атомов водорода, способных к образованию водородной связи в 3 раза больше, чем в молекулах одноатомных спиртов. Поэтому, сила межмолекулярной связи в случае глицерина гораздо больше, чем в молекулах одноатомных спиртов. В случае глицерина необходимо более сильное нагревание, более высокая температура, для того чтобы ослабить связи между молекулами до такой степени, чтобы они перешли в газообразное состояние. По этой причине многоатомные спирты более вязкие и температуры кипения их выше, чем у соответствующих одноатомных спиртов.
Вывод: число гидроксогрупп обуславливает физические свойства (за счет водородных связей).
2.3. Химические свойства многоатомных спиртов.
Предлагаем предсказать химические свойства глицерина. По аналогии с одноатомными спиртами называются реакции горения, замещения водорода гидроксогруппы на щелочной металл, обмен всей гидроксогруппы на галоген и др. Делаем вывод об общности свойств глицерина с одноатомными спиртами, обусловленных функциональной группой ОН. (SMART-слайд № 18).
Затем решаем вопрос: Должно ли вызвать появление новых химических свойств увеличение числа гидроксогрупп в молекулах многоатомных спиртов? (SMART-слайд № 19).
Запись уравнения реакции с HNO3 (азотная кислота) (SMART-слайд № 20).
В 1846 году итальянский химик Асканьо Собреро нагрел глицерин со смесью серной и азотной кислотой. Полученный продукт при выделении взрывался с огромной силой. Так был открыт сложный эфир глицерина и азотной кислоты – тринитрат глицерина (нитроглицерин).
Это вещество пробовали применять в военных целях. Однако такая взрывчатка часто взрывалась раньше, чем требовалось: при транспортировке, от сотрясения и удара. Решение проблемы предложил шведский инженер-химик, изобретатель промышленник Альфред Нобель, который значительную часть жизни прожил в России. (SMART-слайд № 21).
Именно здесь он работал директором завода по производству нитроглицерина. Частые несчастные случаи на заводе побудили Нобеля к поиску методов безопасного обращения с этим веществом. В 1866 году ученый обнаружил, что пропитанная нитроглицерином инфузорная земля (кизельгур – нем. – рыхлая, легкая, пористая) безопасна при хранении и транспортировке, но сохраняет свои взрывчатые свойства. Так был изобретен динамит – его разрушительную силу используют при прокладке туннелей, поиске и добыче полезных ископаемых, в строительстве и военном деле.
Но ... нитроглицерин не только убивает … и лечит: 1% раствор сосудорасширяющее средство (кардиологическое средство) не обладает взрывчатыми свойствами.
Человечество вспоминает с благодарностью о Нобеле как и об основателе знаменитой премии (завещание Нобеля).
2.4. Демонстрация качественной реакции многоатомных спиртов.
Ответ на него учащиеся получают при демонстрации опыта – действия глицерина на гидроксид меди (II). Отмечается, что многоатомные спирты в отличие от одноатомных спиртов реагируют с нерастворимым основанием и легче окисляются. Взаимодействие глицерина с основанием говорит о том, что многоатомные спирты обладают слабыми кислотными свойствами.
Записываем уравнение реакции глицерина с гидроксидом меди (II) ( SMART-слайд № 22).
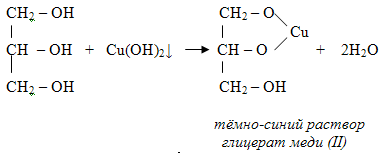
Итак, мы рассмотрели отличительные свойства многоатомных спиртов. Вернёмся к вопросу исследования содержания многоатомных спиртов в жевательных резинках.
2.5. Исследование содержания многоатомных спиртов в жевательной резинке (SMART-слайд № 23).
Вопрос: Каким реактивом мы можем обнаружить сорбит, ксилит, маннит?
Ответ: Свежеприготовленным гидроксидом меди (II).
Опыт 2.
1) Приготовление контрольного образца:
В один хим. стакан + 3-4 капли CuSO4+ 1 мл NaOH → осадок синего цвета
2) Обнаружение сорбита (ксилита, маннита) в жевательной резинке:
В другой хим. стакан + 3-4 капли CuSO4+ 1 мл NaOH → осадок синего цвета + добавить (немного) взвесь из опыта 1→ тёмно-синий раствор.
Вывод: жевательные резинки (любые) содержат многоатомные спирты: сорбит, ксилит, маннит.
Задание: Составьте уравнение реакции взаимодействия ксилита с гидроксидом меди (II).
3. Подведение итогов урока. Вывод (SMART-слайд № 24).
- Во всех многоатомных спиртах гидроксильные группы находятся при разных атомах углерода;
- Число гидроксогрупп влияют на физические свойства спирта (за счет водородных связей);
- Общие свойства с одноатомными спиртами обусловлено наличием функциональной группой ОН;
- На примере многоатомных спиртов ещё раз убеждаемся в том, что количественные изменения переходят в изменения качественные: накопление гидроксильных групп в молекуле обусловило в результате их взаимного влияния появление у спиртов новых свойств по сравнению с одноатомными спиртами – взаимодействие с нерастворимыми основаниями.
4. Домашнее задание (SMART-слайд № 25).
- § 16, ученика «Химия 10 класс» под редакцией О.С.Габриеляна.
- Творческое задание:
- составить кроссворд;
- написать реферат об Альфреде Нобеле;
- составить презентацию о применении нитроглицерина.
5. Закрепление учебного материала (тестовый контроль) (SMART-слайд № 26).