Квантовые постулаты Бора. Модель атома водорода по Бора
Тип урока: Урок конструирования знаний.
Цели:
- Ввести учащихся в процесс отыскания противоречий между законами классической физики и постулатами Бора.
- Обеспечить выдвижение учащимися гипотезу, объясняющую стабильность атома.
- Объяснить линейчатый спектр излучения атома водорода.
Оборудование: Мультимедийное сопровождение.
Ход урока
- Организационный момент.
- Проверка домашнего задания, ответы на вопросы:
- с какой целью был поставлен опыт Резерфорда, какие были сделаны выводы из этих опытов;
- планетарная модель атома.
- Изучение нового материала:
- неприменимость законов классической физики к явлениям, происходящим внутри атома;
- постулаты Бора;
- спектр излучения атома водорода;
- трудности теории Бора.
- Подведение итогов урока.
Из опытов Резерфорда непосредственно вытекает планетарная модель атома. В центре расположено положительно заряженное атомное ядро, в котором сосредоточена почти вся масса атома. В целом атом нейтрален. Поэтому число внутриатомных электронов, как и заряд ядра, равно порядковому номеру элемента в периодической системе. Ясно, что покоиться электроны внутри атома не могут, т.к. они упали бы на ядро. Они движутся вокруг ядра, подобно тому, как планеты обращаются вокруг Солнца. Такой характер движения электронов определяется действием кулоновских сил со стороны ядра.
В атоме водорода вокруг ядра обращается всего лишь один электрон. Ядро атома водорода имеет положительный заряд, равный по модулю заряду электрона, и массу примерно в 1836,1 раза большую массы электрона. Это ядро названо протоном и стало рассматриваться как элементарная частица. Размер атома - это радиус орбиты его электрона.

На основе этой модели нельзя объяснить факт существования атом, его устойчивость. Ведь движение электронов по орбитам происходит с ускорением, причем весьма немалым.
Ускоренно движущийся заряд по законам электродинамики Максвелла должен излучать электромагнитные волны с частотой, равной частоте его обращения вокруг ядра. Излучение сопровождается потерей энергии. Теряя энергию, электроны должны приблизиться к ядру. Как показывают строгие расчёты, основанные на механике Ньютона и электродинамике Максвелла электрон за ничтожно малое время (порядка 10-8с) должны упасть на ядро. Атом должен прекратить свое существование.
В действительности ничего подобного не происходит. Атомы устойчивы и в невозбужденном состоянии могут существовать неограниченно долго, совершенно не излучая электромагнитные волны.
Не согласующийся с опытом вывод о неизбежной гибели атома вследствие потери энергии на излучение - результат применения законов классической физики к явлениям, происходящим внутри атома. Отсюда следует, что к явлениям атомных масштабов законы классической физики неприменимы.
Выход из крайне затруднительного положения в теории в теории атома был найден в 1913 г. датским физиком Нильсом Бором. На пути дальнейшего развития квантовых представлений о процессах в природе.
Последовательной теории атома Бор, однако, не дал. Он в виде постулатов сформулировал основные положения новой теории. Причём и законы классической физики не отвергались им безоговорочно. Новые постулаты, скорее, налагали лишь некоторые ограничения, на допускаемые классической физикой движения.[1]
Первый постулат Бора (постулат стационарных состояний) [2]:
В атоме существуют стационарные (не изменяющиеся со временем) состояния, в которых он не излучает энергии. Стационарным состояниям атома соответствуют стационарные орбиты, по которым движутся электроны. Движение электронов по стационарным орбитам не сопровождается излучением электромагнитных волн.
В стационарном состоянии атома электрон, двигаясь по круговой орбите, должен иметь дискретные квантованные значения момента импульса, удовлетворяющие условию [2]:
![]() (n = 1, 2, 3, … )
(n = 1, 2, 3, … )
где - me - масса электрона, ![]() - его скорость по n-й орбите радиуса rn,
- его скорость по n-й орбите радиуса rn, 
Второй постулат Бора(правило частот) [2]:
При переходе электрона с одной стационарной орбиты на другую излучается (поглощается) один фотон с энергией:
hv = En - Em
равной разности энергий соответствующих стационарных состояний.
При Em< En происходит излучение фотона, при Em> En - его поглощение. Набор возможных дискретных частот h = (En - Em)/h квантовых переходов и определяет линейчатый спектр атома.
Спектр излучения атома водорода
Постулаты, выдвинутые Бором, позволили рассчитать спектр атома водорода и водородоподобных систем-систем, состоящих из ядра с зарядом Ze и одного электрона, а также теоретически вычислить постоянную Ридберга.
Следуя Бору, рассмотрим движение электрона в водородоподобной системе, ограничиваясь круговыми стационарными орбитами.
Выражение для радиуса n-й стационарной орбиты [2]:
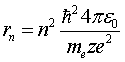 , где n = 1, 2, 3, …
, где n = 1, 2, 3, …
Из этого выражения следует, что радиусы орбит растут пропорционально - -квадратам целых чисел.
Для атома водорода(Z=1) радиус первой орбиты электрона при n =1, называемый первым Боровским радиусом (а) равен [2]
 = 0,528
= 0,528![]() 10-10 м = 52,8
пм
10-10 м = 52,8
пм
Учитывая квантованные для радиуса n-й стационарной орбиты, энергия электрона может принимать только следующие дозволенные дискретные значения [2]:
 (n = 1, 2, 3, …)
(n = 1, 2, 3, …)
Согласно теории Бора при движении электрона по ближайшей к ядру дозволенной орбите атом находится в основном состоянии, являющимся наиболее устойчивым. В основном состоянии атом может находиться неограниченно долгое время, поскольку это состояние соответствует наименьшему возможному энергетическому уровню атома. Когда электрон движется по какой-либо другой из дозволенных орбит, состояние атома называется возбужденным. Через небольшое время (порядка 10-8с) атом самопроизвольно переходит из возбужденного состояния в основное, излучая при этом квант энергии. На рисунке 2 изображена схема атома водорода, на которой показаны возможные орбиты электрона [2].
 , откуда частота излучения
, откуда частота излучения
 , где
, где 
R=3,29×1015с-1 - постоянная Ридберга.
На рисунке 1 изображены энергетические уровни атома водорода, соответствующие различным орбитам электрона. Из рисунка видно, что при переходе электрона с более высоких орбит на первую освобождается энергии гораздо больше, чем при переходе на вторую. Это объясняет, почему серия Лаймана лежит в ультрафиолетовой части спектра, а серия Бальмера - в видимой части.
Энергетические уровни атома водорода

Рис. 1. Энергетические уровни атома водорода.
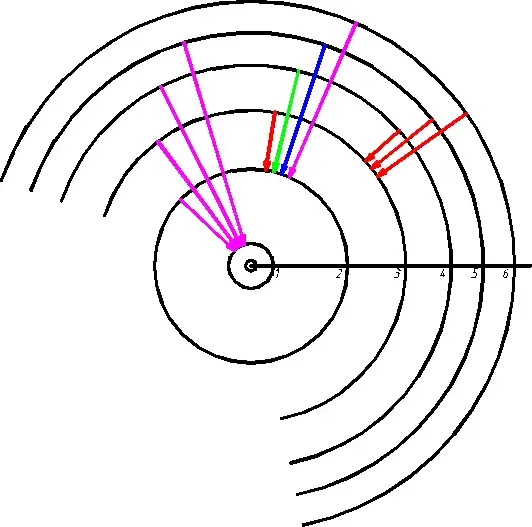
Рис. 2. Дозволенные орбиты электрона в атоме водорода (стрелками указаны возможные переходы электрона с одной орбиты на другую).
Спектр поглощения атома водорода является линейчатым, но содержит только серию Лаймана. Он также объясняется теорией Бора. Так как свободные атомы водорода обычно находятся в основном состоянии (стационарное состояние с наименьшей энергией при n=1), то при сообщении атомам извне определённой энергии могут наблюдаться лишь переходы атомов из основного состояния в возбуждённое (возникает серия Лаймана).
Теория Бора была крупным шагом в развитии атомной физики и являлась важным этапом в создании квантовой механики. Однако эта теория обладает внутренними противоречиями (с одной стороны применяет законы классической физики, а с другой - основывается на квантовых постулатах). Она рассмотрела спектры атома водорода и водородоподобних систем и вычислила частоты спектральных линий, однако не смогла объяснить их интенсивности и ответить на вопрос: почему совершаются те или иные переходы? Серьёзным недостатком теории Бора была невозможность описания с её помощью спектра атома гелия - одного из простейших атомов, непосредственно следующего за атомом водорода.
Итог урока:
- Разъясните смысл постулатов Бора. Как с их помощью объясняется линейчатый спектр атома водорода?
- Найти наибольшую длину волны в ультрафиолетовом спектре водорода. [4]
Использованная литература:
- Физика: Учеб. для 11 кл. общеобразоват. учреждений / Г.Я Мякишев, Б.Б.Буховцев. - 9-е изд. - М.: Просвещение, 2002. - 336 с.
- Трофимова Т.И. Курс физики: Учеб. пособие для вузов. - 2-е изд., перераб. и доп. - М.: Высш. шк., 1990. - 478 с.
- Жданов Л.С. Учеб. по физике для средних специальных учеб. заведений. - М.: Наука, 1975. - 592 с.
- Рымкевич А.П. Физика. Задачник. 10-11 кл.: Пособие для общеобразоват. учеб. заведений. - 5-е изд., перераб. - М.: Дрофа, 2001. - 192 с.