«Ни один сосуд не вмещает больше своего объёма, кроме сосуда знаний – он постоянно расширяется.»
Арабская пословица
Тип урока: Усвоение новых знаний.
Технология: Технология развития критического мышления, деятельностная.
Метапредмет: «Знание».
Форма урока: Урок-исследование.
Цели урока:
- Образовательная – Формирование знаний учащихся о химических свойствах кислот, совершенствование умений наблюдать и применять знания на практике;
- Воспитательная – Демонстрация учащимся необходимости изучения свойств веществ для объяснения различных процессов происходящих в жизни, воспитание положительной мотивации учения, адекватной самооценки;
- Развивающая – Совершенствование умений экспериментировать, наблюдать, анализировать, делать выводы, умения слушать и слышать, умения работать в паре, развитие логического мышления, самостоятельности, способности к рефлексии.
Ожидаемые результаты: Учащиеся умеют составлять уравнения химических реакций; знают химические свойства кислот (соляной или серной); умеют пользоваться таблицей растворимости; умеют пользоваться электрохимическим рядом напряжений металлов; решают экспериментальные задачи по теме.
Организация рабочего места (оборудование и реактивы)
для учащихся
- таблица растворимости, таблица «Кислоты, их соли», пробирки №1 – р-р хлорида натрия, №2 – р-р соляной кислоты, №3 – р-р гидроксида натрия, лакмус;
- Вариант 1: раствор соляной кислоты, гранулы цинка, опилки железа, медная проволока; штатив с пробирками;
- Вариант 2: порошок оксида меди (II), раствор серной кислоты, спиртовка, спички, пробиркодержатель, пробирки;
- Вариант 3: раствор гидроксида натрия, фенолфталеин, раствор соляной кислоты, пробирки;
- Вариант 4: растворы хлорида бария и карбоната натрия, раствор серной кислоты, пробирки.
для учителя
- ПК, проектор, интерактивная доска, видеопрезентация, раствор соляной кислоты, концентрированная серная кислота, вода, индикаторы, штатив с пробирками, химический стакан, стеклянная палочка.
На всех этапах урока используется подготовленная видеопрезентация. Лабораторные опыты выполняются в парах по четырём вариантам.
Слайд 1
Оргмомент
Психоэмоциональная подготовка к уроку: Я рада видеть всех вас на уроке. Оцените своё настроение (смайлики). На уроке мы становимся исследователями, делаем для себя открытие неизвестного.
I. Вызов
Обращение к знаниям учащихся:
Объектом изучения науки химии являются вещества. Какие классы неорганических соединений вы уже знаете? Что такое оксиды? Что такое основания? Что такое кислоты?
Слайд 2
Выполните задание:
K2O, Fe(OH)2, H2S, H3PO4, NaOH, Al2O3, Cu(OH)2, HCI, N2O5, H2SiO3↓, CaO, CO2
Кластер
Из данного перечня выберите формулы только кислот. Составление кластера: Что вы уже знаете о кислотах (состав, классификация, физические свойства). А что вы ещё хотели бы узнать о кислотах? (химические свойства). И так, тема урока «Химические свойства кислот».
Слайд 3
II. Осмысление новой информации
Как можно распознать кислоты? Что такое индикаторы? Какие индикаторы вам известны?
Демонстрационный опыт: в трех химических стаканах находится соляная кислота. Прильем в стаканы индикаторы. Как изменилась окраска растворов?
Кластер
Какой вывод можно сделать? (кислоты можно обнаружить с помощью индикаторов).
Слайд 4
Прочитайте текст «Грелка Вуда».
Выдающийся американский физик и изобретатель Роберт Вуд всегда пытался найти практическое применение различным физическим и химическим явлениям. Раз зимой он отправился со своей невестой покататься на санях. Вот как сам Вуд описал эту поездку:
«У неё замёрзли руки, и я сказал:
- Хорошо бы достать бутылку с горячей водой!
- Замечательно! Только где же мы её возьмём?
- Я сейчас сделаю её, - ответил я и вынул из под сидения винную бутылку, на три четверти заполненную водой. Потом оттуда же флакон с серной кислотой и налил немного похожей на сироп жидкости в воду. Через десять секунд бутылка так нагрелась, что её нельзя было держать в руках. Когда она начинала остывать, я добавлял ещё кислоты. Таким способом бутылка была нагрета всю поездку».
О чём говорится в тексте? Как правильно растворить кислоту? На уроках химии мы часто будем пользоваться разбавленными кислотами.
Демонстрационный опыт: Разбавление концентрированной серной кислоты.
Слайд 5
(ТБ) В химической лаборатории нужно осторожно обращаться с веществами. Работать будем в парах по вариантам.
Лабораторная работа в парах
Слайд 6
После выполнения работы, один ученик от каждого варианта выходит к доске, записывает уравнения реакции и составляет схемы. В это время второй ученик описывает свои наблюдения.
Задание 1 (для всех вариантов): Вам даны пробирки №1, №2, №3. При помощи индикатора распознайте кислоту. По какому признаку распознали кислоту? (пробирка №2)
Задание 2:
Кластер
Вариант 1. Взаимодействие кислот с металлами. В три пробирки поместитесоответственно цинк, железо, медь. Прилейте одинаковое количество соляной кислоты. Что наблюдаете? Какой вывод можно сделать? (не все металлы реагируют с кислотами).
Запишите соответствующие уравнения реакций:
Zn + 2HCl = ZnCl2 + H2↑ (реакция замещения)
Fe + 2HCl = FeCl2 + H2↑ (реакция замещения)
Cu + HCl ≠
При пайке, например электропроводов, используется первая реакция.
Практическим путем учеными было выяснено, какие металлы вытесняют водород из растворов кислот. Таким образом был составлен ряд Н.Н.Бекетова, который сейчас называют электрохимический ряд напряжения металлов. Если металл находится до водорода, то он реагирует с кислотами, если после, то – нет.
Кластер
Вариант 2. Взаимодействие кислот с оксидами металлов. В сухую пробирку поместите небольшое количество оксида меди (II), прилейте 2 мл раствора серной кислоты.
Осторожно нагрейте пробирку, соблюдая правила техники безопасности. Что наблюдаете? Составьте уравнение реакции. Какие вещества образуются в результате реакции?
CuO + H2SO4 = CuSO4 + H2O (реакция обмена)
Кластер
Вариант 3. Взаимодействие кислот с основаниями. В пробирку налейте немного раствора гидроксида натрия и прибавьте 1-2 капли фенолфталеина. Что вы наблюдаете?
К раствору щелочи с фенолфталеином приливайте по каплям соляную кислоту, периодически взбалтывая содержимое пробирки. Что вы наблюдаете? Составьте уравнение реакции.
NaOH + HCl = NaCl + H2O (реакция обмена)
Кластер
Вариант 4. Взаимодействие кислот с солями. В две пробирки прилейте соответственно растворы хлорида бария и карбоната натрия. Прилейте в обе пробирки серную кислоту. Что наблюдаете? (выпадения осадка белого цвета; выделение пузырьков газа). Напишите уравнение химической реакции.
BaCl2 + H2SO4 = BaSO4 + 2HCl (реакция обмена)
Na2CO3 + H2SO4 = Na2SO4 + H2O + CO2↑ (реакция обмена)
Газированную воду можно считать слабой угольной кислотой, которая сразу разлагается на углекислый газ и воду.
Составление опорного конспекта:
кислота + |
металл |
с о л ь |
+ |
Н2 |
основный оксид |
Н2О |
|||
основание |
Н2О |
|||
соль |
кислота |
Слайд 7
Закрепление: Пользуясь опорным конспектом (схемой), допишите уравнения реакций:
Мg + HCl →
СaО + HCI →
KОH + HCI →
III. Рефлексия
Слайд 8
Выполните задание: Выберите правильный ответ, расставьте точки на оси координат, соедините последовательно точки:
Вопросы |
да |
нет |
1. Серебро реагирует с раствором соляной кислоты |
2;2 |
2;1 |
2. При взаимодействии железа с раствором серной кислоты выделяется водород |
8;1 |
8;2 |
3. В растворах кислот лакмус имеет синий цвет |
7;6 |
6;6 |
4. При разбавлении кислоту нужно вливать в воду |
6;9 |
7;9 |
5. Угольная кислота неустойчивая, разлагается на углекислый газ и воду |
4;9 |
4;8 |
6. При взаимодействии кислоты и основания образуется соль и вода |
4;6 |
6;4 |
Слайд 9,10
Ответ: Рисунок «Колба». Колба – это химический сосуд. Как гласит арабская пословица «Ни один сосуд не вмещает больше своего объёма, кроме сосуда знаний – он постоянно расширяется».
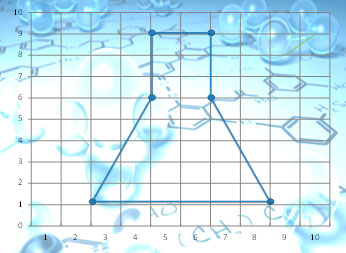
Рис. №1. Ответ на задание 5 «Колба»
Работа с кластером.
- Что нового вы узнали о кислотах? Чему научились?
Слайд 11
Домашнее задание (на листах):
1. § 32. Упр.7, 8 с.91.
2. Исследовательское задание. Опыт с лимонным соком.
Разрежьте лимон и выдавите немного лимонного сока на блюдце, на листе бумаги сделайте им надпись или рисунок. После высыхания прогладьте горячим утюгом. Опишите свои наблюдения:
| Что делали? | Что наблюдали? |
Где можно использовать? |
|
|
|
- Довольны ли вы своей работой на уроке? Работа с кластером.
- Что нового вы узнали о кислотах?
- Довольны ли вы своей работой на уроке?
Слайд 12- Оцените своё настроение (смайлики).
Слайд 13 - Спасибо за урок!
Литература
для ученика
- Рудзитис Г.Е., Фельдман Ф.Г. Химия 8 класс. М.: «Просвещение», 2011г.
- Домашние химические опыты – Режим доступа: http://chimikschool.jimdo.com – 14.01.2014 г.
для учителя
- Рудзитис Г.Е., Фельдман Ф.Г. Химия 8 класс. М.: «Просвещение», 2011г.
- Гара Н.Н. Сборник программ образовательных учреждений «Химия» 8-9, 10-11 классы. М.: «Просвещение», 2011г.
- Днепров Э.Д., Аркадьев А.Г. Сборник нормативных документов «Химия». М.: «Дрофа», 2007г.
- Аранская О.С., Бурая И.В. Проектная деятельность школьников в процессе обучения химии 8-11 классы. М.: «Вентана-Граф», 2005г.
- Оржековский П.А., Давыдов В.Н., Титов Н.А. Экспериментальные творческие задачи по неорганической химии: Книга для учащихся. (Методическая библиотека.) – М: АРКТИ, 1998. – 48 с.: ил.
- Григорьева Э.С. Использование технологии критического мышления на уроках химии" – Режим доступа: https://urok.1sept.ru/articles/528850/ - 25.12.2013 г.
- Техника безопасности в кабинете химии. Рисунки – Режим доступа: http//rusanova.nm.ru/tb.html – 14.01.2014 г.