Изучаемая в 10 классе тема «Измерение скоростей молекул газа» может явиться неплохой иллюстрацией к изложению отдельных вопросов катихитической методики обучения. В противовес уменьшению количества часов отведённых на изучение физики, педагоги должны искать наиболее оптимальные и эффективные методики преподавания. Например, это может быть изучение материала блоками, где предусмотрено рассмотрение уже обобщённого материала и приведены необходимые дополнения, замечания и частные случаи.
Так данная тема может входить в блок «Идеальный газ».
РАЗДАТОЧНЫЙ ЛИСТ №1
60. Идеальный газ (§61) – модель реального газа, газ, взаимодействие между молекулами которого пренебрежимо мало (или газ, состоящий из молекул, не взаимодействующих друг с другом и имеющих нулевые размеры). Молекулы газа можно рассматривать как материальные точки, взаимодействие которых происходит только при их столкновении (притяжения нет, а при столкновении проявляется отталкивание).
Постулаты МКТ идеального газа
- В любом макроскопическом объёме газа число молекул очень велико.
- Размеры молекул пренебрежимо малы по сравнению с расстояниями между ними.
- Распределение молекул в объёме должно мало отличаться от равномерного.
- Все соударения являются абсолютно упругими (т. е. как будто молекулы – маленькие твёрдые шарики).
- Молекулы взаимодействуют друг с другом или со стенкой сосуда только в момент соударения.
- Молекулы находятся в непрекращающемся хаотическом движении. (Все направления движения молекул равноправны.)
- К движению отдельной молекулы применимы законы механики Ньютона.
- Модель не применима при высоких давлениях, а также при очень низких температурах.
61. Давление газа в МКТ – результат ударов молекул о стенку,.§61.При измерении давления фиксируется средняя по времени сила, действующая на каждую квадратную единицу площади поверхности. (Давление р = F/S, Па (паскаль), 1Па = 1Н/м2.)
62..Для определения среднего давления нужно знать среднее значение квадрата скорости молекул – ![]() . §62. Скорости молекул беспорядочно меняются (в результате столкновений), но средний квадрат скорости вполне определённая величина (для разных температур). Ведь средний рост учеников в 8 и 10 классах отличаются, хотя и там, и там могут быть ученики и высокого, и низкого роста.
. §62. Скорости молекул беспорядочно меняются (в результате столкновений), но средний квадрат скорости вполне определённая величина (для разных температур). Ведь средний рост учеников в 8 и 10 классах отличаются, хотя и там, и там могут быть ученики и высокого, и низкого роста.
63. Основное уравнение МКТ газов, §63.
![]() p – давление, Па; mo – масса молекулы, кг; n = N/V – концентрация –число частиц в единице объёма (в «СИ» 1 м3), м–3; N – число частиц, (безразмерная величина); V – объём, м3;
p – давление, Па; mo – масса молекулы, кг; n = N/V – концентрация –число частиц в единице объёма (в «СИ» 1 м3), м–3; N – число частиц, (безразмерная величина); V – объём, м3; ![]() – средний квадрат скорости. ⅓ в формуле – отражение трёхмерности пространства, то есть у вектора скорости существуют 3 проекции. Формула связывает макроскопическую величину – давление, которое может быть измерено манометром, – с микроскопическими величинами, характеризующими молекулы: масса, скорость хаотичного движения.
– средний квадрат скорости. ⅓ в формуле – отражение трёхмерности пространства, то есть у вектора скорости существуют 3 проекции. Формула связывает макроскопическую величину – давление, которое может быть измерено манометром, – с микроскопическими величинами, характеризующими молекулы: масса, скорость хаотичного движения.
Давление идеального газа пропорционально произведению концентрации молекул и средней кинетической энергии поступательного движения молекул:
, где
РАЗДАТОЧНЫЙ ЛИСТ №2
64. Макроскопические параметры – величины, характеризующие состояние макроскопических тел без учёта их молекулярного строения (объём V, давление р, температура Т, t и др.), §64.
65. Тепловое равновесие – состояние тел, при котором все макроскопические параметры сколь угодно долго остаются неизменными. В системе не меняются V, р, нет теплообмена, нет взаимных превращений газов, жидкостей и твёрдых тел и т.д.
66. Температура характеризует состояние теплового равновесия системы тел: все тела системы, находящиеся друг с другом в тепловом равновесии, имеют одну и ту же температуру.
![]() – постоянно для газов в состоянии теплового равновесия и пропорционально Т.
– постоянно для газов в состоянии теплового равновесия и пропорционально Т.
![]() (1), где Т – абсолютная температура, К (кельвин);
(1), где Т – абсолютная температура, К (кельвин);
1К = 10С, то есть величина кельвина и градуса Цельсия равны;
изменение температуры по разным шкалам: ΔТ(К) =Δ t (0С). §66.
Абсолютная шкала температур (англ., У. Кельвин, 1824-1907 ) или шкала Кельвина: абсолютный нуль температуры Т = 0 (если в уравнении (1) р= 0 или V= 0) – предельная температура, при которой давление идеального газа обращается в 0, при фиксированном объёме или при которой объём идеального газа стремится к 0 при неизменном давлении. Т < 0 не может быть, так как в (1) р,V, N не могут быть < 0.
Т(К) = t (oС) + 273 (oС) => (абсолютному 0 – минимальной температуре) Т = 0 соответствует t = – 273 oС.
Для шкалы Цельсия за 0 взята температура таяния льда, а 100 oС – температура кипения воды при норм. атмосферном давлении.
Температура – мера средней кинетической энергии движения молекул.§66.
.
Средняя кинетическая энергия хаотичного поступательного движения молекул газа пропорциональна абсолютной температуре. (Формула справедлива и для жидкостей, и для твёрдых тел).
Постоянная Больцмана (австр., Людвиг Больцман, 1844-1906)
k = 1,38 ∙10–23Дж/К – коэффициент, переводящий температуру из градусной меры (К) в энергетическую (Дж) и обратно.
Из (1), так как n = N/V => р = nkT , при одинаковых давлениях и температурах концентрация у всех молекул газов одна и та же =>
Закон Авогадро (химия): в равных объёмах газов при одинаковых температурах и давлениях содержится одинаковое число молекул.
67. Средняя квадратичная скорость, §67. (Из ![]() и
и ![]() .)
.)
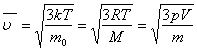 , R = k ∙ NA = 8, 31Дж/(моль∙К) – универсальная газовая постоянная.
, R = k ∙ NA = 8, 31Дж/(моль∙К) – универсальная газовая постоянная.
Скорости быстрее снаряда: при 0oС для молекулы азота 500м/с, для водорода – 1800м/с.
Опыты Штерна (нем., О. Штерн в 1920 г.).
,
где RВ – радиус внешнего цилиндра, RА – радиус внутреннего цилиндра, n – число оборотов в секунду, s – среднее смещение полоски серебра, вызванное вращением прибора (здесь также приводится рис. 9. 5 г [1]).
Изучение материала в условиях дефицита времени проводится следующим образом: каждый раздаточный лист соответствует одному уроку, когда обучающиеся знакомятся с темой по презентации, а затем делают опорные записи в тетради. При этом текст на раздаточных листах, выделенный курсивом, предназначен только для чтения. При необходимости эти листы ученики могут забрать домой. В тексте указаны параграфы учебника, что удобно при более детальной самостоятельной проработке темы учащимися уже дома. Кроме того, наличие таких раздаточных листов очень удобно для восполнения пробелов в знаниях, возникающих в результате пропущенных уроков, а также при работе с детьми, находящихся на домашней форме обучения. Закрепление и углубление понимания изучаемого материала производится на уроках решения задач.
В рассматриваемом примере тема «Измерение скоростей молекул газа» выносится на отдельный урок, хотя с пропедевтической целью, для создания завершённого обзора изучаемого раздела, основной материал был внесен в п. 67 листа №2.
Поэтому на уроке изучения основного материала пункт 67 рассматривается обзорно: у молекул газа большие скорости, которые можно вычислить по формулам или определить экспериментально.
Урок «Измерение скоростей молекул газа» проводится с использованием презентации, построенной на основе катихитического способа обучения.
То есть учитель, пользуясь сведениями о степени подготовки своих учеников и уровне их развития, пытается не просто дать некую сумму знаний, а вызвать интерес обучаемых к происходящему через диалог, через некую заранее спланированную систему «вопрос – ответ», с целью формирования, обобщения, более глубокого усвоения или закрепления материала вынесенного на данное занятие. С помощью чётко поставленных и правильно подобранных вопросов, что легко достигается при создании презентации с её последовательно расположенными слайдами, учитель даёт возможность ученикам переходить от одной истины к другой, близко с ней связанной, не в процессе простого восприятия излагаемого материала, а в результате попыток самостоятельно проанализировать предлагаемую ситуацию и высказать собственное мнение или предложить своё решение. Для этого разбор учебного материала должен идти так, чтобы неизвестное вытекало из прежде усвоенного учащимися или было доступно для генерации идей отдельными членами детского коллектива. При этом относительно часто выясняется, что наиболее догадливым на уроке может стать далеко не отличник, что становится для ученика положительным стимулом, включающим обучаемого в дальнейшую работу.
Таким образом, катихитический способ обучения предполагает наличие у педагога специально продуманных и систематизированных вопросов по изучаемой теме. Это не может быть совокупность бессистемных, расположенных в случайном порядке заданий. То есть учитель, опираясь на усвоенные учащимися знания, ставит такие вопросы и придаёт им такую форму, чтобы обучаемый чувствовал посильность данного задания и стремился проявить свои знания и способности, при этом постигая для себя что-то новое [2].
Данная методика напоминает технологию проблемного обучения, которая по степени познавательной активности и самостоятельности производится в трёх основных формах:
1) проблемное изложение (осуществляется преподавателем, делающего учеников как бы соучастниками научного поиска);
2) частично-поисковая деятельность;
3) самостоятельная исследовательская деятельность.
При частично-поисковой деятельности работа обучаемых направляется педагогом с помощью специальных вопросов, побуждающих учеников к самостоятельным рассуждениям и поиску ответа на отдельные части поставленной проблемы. Но, как и у всякой методики, здесь есть свои минусы: большие затраты времени на получение запланированного результата и слабая управляемость познавательной деятельностью учащихся. Катихитический же способ предполагает поэтапный переход от вопроса к вопросу и постепенное подведение учащихся к ключевым идеям урока. Если же какие-то понятия достаточно сложны, то они вводятся без нерациональной траты времени на поиски верного ответа. Конечно, здесь есть свои сложности. Например, сохранение темпа урока и предоставление возможности ученику дать полный и развёрнутый ответ. Кроме того, наиболее интересным с методической точки зрения будет урок, где учитель сможет найти оптимальный вариант из вопросов требующих трёх уровней деятельности: репродуктивной (развивающей память), частично-поисковой (развивающей логическое мышление) и творческой (воспитывающей генераторов идей). Такие вопросы рассмотрены в данной презентации, причём по возможности задания или ответы сопровождаются зрительными образами, которые или подводят к ответу, или закрепляют в памяти учащегося полученную информацию. Это очень важно, так как значительная часть имеющихся у нас знаний получена именно посредством зрения. Но особенно это актуально для современных детей, приученных уже к клиповому восприятию и мышлению.
Примеры из презентации
I этап
1. Идеальным газом называется…
модель реального газа, где молекулы газа рассматривают как материальные точки, взаимодействие между которыми происходит только при столкновении.
2. Объясните своими словами содержание понятия «идеальный газ».
3. При каких условиях реальный газ можно заменить моделью «идеальный газ»?
4. При каких условиях реальный газ нельзя считать идеальным?
Подсказка: концентрация, давление, температура.
5. Будут ли различаться физические свойства различных разреженных газов, если к ним применима одна и та же модель – идеальный газ?
II этап
1. Средние скорости молекул превышают скорость звука и достигают сотен м/с. Почему же запах духов в комнате из одного угла в другой распространяется достаточно медленно (порядка десятков секунд)?
2. Как изменится средняя квадратичная скорость движения молекул при увеличении температуры в 4 раза?
3. Какие молекулы в атмосфере движутся быстрее: молекулы азота или молекулы кислорода? [1].
4. Во сколько раз средняя квадратичная скорость молекул кислорода меньше, чем у молекул водорода? Температуры одинаковы.
III этап
1. Почему в опыте Штерна полоска серебра: а) смещена; б) размыта по краям; в) неоднородна по толщине?
2. При вращении прибора Штерна с частотой 45 сˉ¹ среднее смещение полоски серебра, обусловленное вращением, составляло 1,12 см. Радиусы внутреннего и внешнего цилиндров равны 1,2 и 16 см. Найти среднюю квадратичную скорость атомов серебра из данных опыта и сравнить её с теоретическим значением, если температура накала платиновой нити равна 1500 К[3].
3. Какой скоростью обладала молекула паров серебра, если её угловое смещение в опыте Штерна составляло 5,4º при частоте вращения прибора 150 сˉ¹ ? Расстояние между внутренним и внешним цилиндрами равно 2 см.
Далее учащимся предлагается рассмотреть и объяснить другой вариант выполнения опыта Штерна и также предлагаются вопросы для закрепления. (Это для физико-математического профиля.)
IV этап
Это вопросы ЕГЭ, тоже снабжённые видеорядом. Наиболее сложный вопрос предваряется вопросами житейского характера. Они, с одной стороны, показывают учащимся универсальность математических подходов к похожим проблемам, что уже было в презентации при рассмотрении графика максвелловского распределения скоростей, а с другой стороны, действительно помогают решить уже сугубо научный вопрос. При этом не возникает эмоционального напряжения и усталости, так как речь вначале идёт о простых вопросах, взятых из жизни.
Предварительные вопросы:
1. Как вы рассчитаете средний возраст членов вашей семьи?
2. Как вы будете вычислять средний возраст учеников в классе, если их можно разбить на 3 возрастные группы: 15, 16 и 17 лет [4]?
Вопрос
В эксперименте получены данные, что при заданной температуре молекулы можно разбить на три группы, обладающие разными скоростями, и распределение по группам представляется в виде диаграммы. Считая, что в каждой группе молекулы движутся со скоростью, соответствующей середине интервала скоростей, оцените среднюю квадратичную скорость всех молекул [5].
Литература:
1. Мякишев Г.Я., Буховцев Б.Б., Сотский Н.Н. Физика – 10. – М.: Просвещение, 2011.
2. Евтушевский В. Методика арифметики. – С.-П.: Типография В. Безобразова и Комп., 1883.
3. Рымкевич А.П. Сборник задач по физике. 10-11 кл. – М.: Дрофа, 2002.
4. Касьянов В.А. Физика-10. – М.: Дрофа, 2005.
5. Орлов В.А. ЕГЭ-2008. Физика. – М.: Интеллект-Центр, 2007.