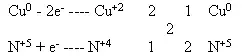"Окислительно-восстановительные реакции. Метод электронного баланса" по технологии модульного обучения
Цели:
- изучить реакции, идущие с изменением степени окисления;
- уяснить понятие степень окисления и как определить степень окисления элемента;
- закрепить навыки и умения в расстановке коэффициентов методом электронного баланса с использованием математических знаний;
- развитие коммуникативных качеств путём использования работы по парам и в группах.
|
№ УЭ |
Содержание учебного материала |
Руководство к освоения |
||||
|
УЭ-1
УЭ-2
УЭ-3
УЭ-4
УЭ-5
УЭ-6 |
Прочитай определение окислительно-восстановительные реакции. Запиши в тетрадь определение ОВР. Заучи. Ответь соседу.
Цель: научиться определять степени окисления элементов. Прочитай определение "степень окисления" и уясните как определяется степень окисления элементов.
Цель: уяснить понятия "окислитель", "восстановитель", "процесс окисления и процесс восстановления". Запиши в тетрадь определения "окислитель", "восстановитель", "процесс окисления и процесс восстановления".
Цель: научиться подбирать стехиометрические коэффициенты методом электронного баланса. Внимательно прочти материал пункта 2.1. Уясни порядок нахождения коэффициентов в уравнении. Сделай конспект. Материал проговори про себя и ответь соседу.
Цель: изучить типы ОВР. Внимательно прочти материал пунктов. Запиши в тетрадь определения типов ОВР. Рассмотри примеры реакций.
Цель: изучить ОВР с использованием дробных степеней окисления. Прочти материал пункта 5.1. Составь конспект. Материал проговори про себя и ответь соседу. Прослушай объяснение учителя.
1.Обязательным условием ОВР является:
2. К ОВР относится процесс, выраженный схемой уравнения:
3. К ОВР не относится:
4. В реакции с HClO4 сульфит натрия выступает:
5. Только окислителем может выступать соединение:
6. Реакция относится к атомно-молекулярным:
7. Одна молекула окислителя в приведенном ниже уравнении присоединяет число электронов: K2Cr2O7 + KI + H2SO4 ---- K2SO4 + I2 + Cr2(SO4)3 + H2O
8. Число электронов, отдаваемых молекулой восстановителя в уравнении: CH2 = CH2 + Cl2 ---- CH2Cl - CH2Cl
9. Сумма коэффициентов левой части уравнения: Al + HNO3 ---- Al(NO3)3 + NH4NO3 + H2O
10. Сумма коэффициентов правой части уравнения: PH3 + KMnO4 + HCl ---- H3PO4 + MnCl2 + KCl + H2O
Подведите итог своей работы. Ответы на тестовые задания сдайте учителю. |
пункт 1.1
пункт 1.2
задание 3.1, 3.2, 3.3, 3.4, 3.5.
пункт 1.3, 1.4, 1.5, 1.6. пункт 1.7, 1.8.
пункт 2.1.
пункт 5.2. пункты 4.1- 4.4
пункт 5.1. |
1. Окислительно-восстановительные реакции
1.1. Окислительно-восстановительные реакции (ОВР) - это реакции, протекающие с изменением степени окисления атомов, входящих в состав реагирующих веществ. В ОВР происходит переход от одних атомов, молекул или ионов к другим.
1.2. Степень окисления - условный заряд атома в молекуле, вычисленный из предположения, что она состоит из ионов. При расчете степени окисления исходят из электроотрицательности молекул: сумма всех степеней окисления атомов в соединении равна нулю. Постоянную степень окисления имеют: Н+1, О-2 , Ме+ по валентности, свободный элемент0.
Определим степени окисления элементов:
| Н2СО3
+2 +4 -6 = 0 |
Н3РО4
+3 +5 -8 = 0 |
1.3. Процесс отдачи электронов атомом, молекулой или ионом называется окислением.
Э - пе ---- Э+п, где Э - восстановитель.
1.4. Процесс присоединения электронов атомом, молекулой или ионом называется восстановлением
Э + пе ---- Э-п, где Э - окислитель.
1.5. Атомы, ионы или молекулы, отдающие электроны называются восстановителями, в результате ОВР они окисляются.
1.6. Атомы, ионы или молекулы, принимающие электроны называются окислителями, при этом они восстанавливаются.
1.7. Окисление всегда сопряжено с восстановлением.
Число электронов, участвующих в процессе окисления равно числу электронов, участвующих в процессе восстановления.
| Типичные окислители | Типичные восстановители |
|
|
1.8. Окислителем или восстановителем, в зависимости от конкретных условий могут выступать:
а) ионы металлов и неметаллов в промежуточной степени окисления. Например:
Fe+2 - 1e- ---- Fe+3, где Fe+2 - восстановитель, реакция окисления;
Fe+3 + 2e- ---- Fe0, где Fe+2 - окислитель, реакция восстановления;
S+4 - 2e- ---- S+6, где S+4 - восстановитель, реакция окисления;
S+4 + 6e- ---- S-2, где S+4 - окислитель, реакция восстановления.
б) элементы главных подгрупп 4 и 5 групп периодической системы элементов.
Например:
C + O2 ---- CO2;
C0 - 4e- ---- C+4, где C0 - восстановитель, реакция окисления;
C + 2H2 ---- CH4;
C0 + 4e- ---- C-4, где C0 - окислитель, реакция восстановления.
2. Методы уравнивания окислительно-восстановительных реакций
2.1. Подбор стехиометрических коэффициентов в ОВР можно проводить методом электронного баланса или методом полуреакций. Рассмотрим подробно метод электронного баланса на примере реакции:
Ca3(PO4)2 + C + SiO2 ---- CaSiO3 + P + CO.
2.2. Порядок нахождения коэффициентов следующий:
а) Определяем элементы, меняющие степень окисления - это Р и С.
б) Составляем электронные уравнения процессов восстановления и окисления, учитывая количество атомов восстановления или окисления в исходных молекулах:
2Р+5 + 10е- ---- 2Р0, процесс восстановления, Р+5 - окислитель.
С0 - 2е- ---- С+2, процесс окисления, С0 - восстановитель.
в) Находим наименьшее общее кратное, чтобы уравнять количество электронов в процессах окисления и восстановления:
г) Подставим найденные коэффициенты в уравнение ОВР:
Ca3(PO4)2 + 5C + SiO2 ---- CaSiO3 + 2P + 5CO.
д) Подбор следующих коэффициентов осуществляем в строгой последовательности:
- Уравниваем катионы, не имеющие степень окисления (в данном случае - Са+2).
- Уравниваем неметаллы, не меняющие степень окисления (в данном случае - Si+4).
- Уравниваем атомы водорода (в данном случае они отсутствуют).
Ca3(PO4)2 + 5C + 3SiO2 ---- 3CaSiO3 + 2P + 5CO
е) правильность подбора коэффициентов проверяем подсчитывая число атомов кислорода в правой и левой частях уравнения.
2.3. В некоторых реакциях кислоты, выступающие как окислитель (или восстановитель), могут выполнять и роль среды, выступая в качестве солеобразователя без изменения степени окисления:
Cu + HNO3 ---- Cu(NO3)2 + NO2 + H2O
Cu + 2HNO3(окислитель) + 2HNO3(солеобразователь) ---- Cu(NO3)2 + 2NO2 + 2H2O
Итоговое: Cu + 4HNO3 ---- Cu(NO3)2 + 2NO2 + 2H2O
2KMnO4 + 10HCl + хHCl(солеобразователь) ---- 2MnCl2 + KCl + 5Cl2 + H2O
Уравниваем катионы металла, не меняющего степень окисления (это К+):
2KMnO4 + 10HCl + хHCl(солеобразователь) ---- 2MnCl2 + 2KCl + 5Cl2 + H2O
Из правой части уравнения следует, что 6 молекул НСl используется для солеобразования, поэтому всего в левой части уравнения должно быть 16 молекул НСl. Осталось уравнять водород:
2KMnO4 + 16HCl ---- 2MnCl2 + 2KCl + 5Cl2 + 8H2O
3. Задания для самостоятельной работы
3.1. Определите степени окисления элементов в следующих веществах и указать окислителем или восстановителем будут они в ОВР:
HClO4, MnO2, HCl, NH3, H2O2, H2S, Na2CrO4, N2O5, PH3, NaJO2.
3.2. Составить электронные уравнения:
| N+5
N+3 N+3 |
---- N+4
---- N+5 ----N+2 |
C0
Mn+7 As+3 |
---- C+4
---- Mn+2 ---- As+5 |
S-2
Al0 Bi+5 |
---- S+4
---- Al+3 ---- Bi+3 |
3.4. Определите степень окисления азота в веществах: N2O4, (NH4)2CO3, NO2-, NH4Cl, N2H4, NH2OH, Pb(NO2)2.
3.5. Определите степень окисления хлора в веществах: KClO3, Cl2, NaClO, Ca(ClO)2, AlCl3.
4. Классификация окислительно-восстановительных реакций
4.1. Реакции межмолекулярного окисления-восстановления - это ОВР, в которых атом-окислитель и атом-восстановитель принадлежат разным веществам. Уравнивание проводим методом электронного баланса:
2HN+3O2 + H2S-2 ---- 2N +2O + S0 + 2H2O
N+3 + 1e- ---- N+2 2 окислитель, восстановление
S-2 ---- 2e- ---- S0 1 восстановитель, окисление
KI+5O3 + 5RI- + 3H2SO4 ---- 3I20 + 3K2SO4 + 3H2O
I+5 + 5e- ---- I0 1 окислитель, восстановление
I-1 - 1e- ---- I0 5 восстановитель, окисление
2KMn+7O4 + 5H2O2-1 + 3H2SO4 ---- 2Mn +2SO4 + 5O20 + K2SO4 + 8H2O
Mn+7 + 5e- ---- Mn+2 2 окислитель, восстановление
2O-1 - 2e- ---- O20 5 восстановитель, окисление
2KMnO4 + 10FeSO4 + 8H2SO4 ---- 5Fe2(SO4)3 + 2MnSO4 + K2SO4 + 8H2O
Mn+7 + 5e- ---- Mn+2 2 окислитель, восстановление
Fe+2 - 1e- ---- Fe+3 5 восстановитель, окисление
Наименьшее общее кратное 5 умножаем на 2, так4 как в продуктах реакции атомов железа должно быть четное количество.
4.2. К этому же типу ОВР можно отнести и реакции межатомного и атомно-молекулярного окисления-восстановления:
Fe0 + S0 ---- Fe+2S-2
Fe - 2e- ---- Fe+2 восстановитель, окисление
S0 + 2e- ---- S-2 окислитель, восстановление
HN +5O3 + Cu0 ---- Cu+2(NO3)2 + 2N+4O2 + 2H2O
Cu0 - 2e- ---- Cu +2 восстановитель, окисление
N+5 + 1e- ---- N+4 окислитель, восстановление
4.3. Реакции внутримолекулярного окисления-восстановления - это ОВР, в которых атом-окислитель и атом-восстановитель входят в состав одной молекулы или иона и могут быть представлены как разными элементами, так и одним элементом, но в разных степенях окисления:
2NaN+5O3-2 ---- 2NaN+3O2 + O20
N+5 +2e- ---- N+3 2 окислитель, восстановление
2O-2 - 4e- ---- O02 1 восстановитель, окисление2KCl+5O3 ---- 2KCl- + 3O20
Cl+5 + 6e- ---- Cl-1 2 окислитель, восстановление
2O-2 - 4e- ---- O20 3 восстановитель, окисление(N-3H4)2Cr2+6O7 ---- N20 + Cr2+3O3 + 4H2O
2N-3 - 6e- ---- N20 1 окислитель, восстановление
2Cr+6 + 6e- ---- 2Cr+3 1 восстановитель, окисление2Hg+2O-2 ---- 2Hg0 + O20
Hg+2 + 2e- ---- Hg0 2 окислитель, восстановление
2O-2 - 4e- ---- O20 1 восстановитель, окислениеN-3H4N+5O3 ---- N2 +1O + 2H2O
N-3 - 4e- ---- N+1 1 окислитель, восстановление
N+5 + 4e- ---- N+1 1 восстановитель, окислениеN-3H4N+3O2 ---- N20 + 2H2O
N-3 - 3e- ---- No 1 окислитель, восстановление
N+3 + 3e- ---- N0 1 восстановитель, окисление2Ag+N+5O3 ---- 2Ag0 + 2N+4O2 + O20
Ag+ + 1e- ---- Ag0 2 окислитель, восстановление
N+5 + 1e- ---- N+4
2O-2 - 4e- ---- 2O0 4 восстановитель, окисление
4.4. Реакция диспропорционирования - это ОВР, в которых роль окислителя и восстановителя выполняют атомы одного и того же элемента, находящегося в промежуточной степени окисления. К этому же типу реакций относят реакции самоокисления-самовосстановления и дисмутации.
Cl20 + H2O ---- HCl- + HCl+O
Cl0 - 1e- ---- Cl+ 1 восстановитель, окисление
Cl0 + 1e- ---- Cl- 1 окислитель, восстановление3HN+3O2 ---- HN+5O3 + 2N+2O + H2O
N+3 + 1e- ---- N+2 1 восстановитель, окисление
N+3 - 2e- ---- N+5 1 окислитель, восстановление2N+4O2 + H2O ---- HN+3O2 + HN+5O3
N+4 + 1e- ---- N+3 1 восстановитель, окисление
N+4 - 1e- ---- N+5 1 окислитель, восстановление
5. Уравнение ОВР с использованием дробных степеней окисления
5.1. Дробная степень окисления элемента свидетельствует о том, что атомы одного и того же элемента находятся в разных степенях окисления, либо вещество представляет собой смесь веществ, в которых элемент находится в разных степенях окисления.
Fe3O4 + 4 CO ---- 3Fe + 4CO2
3Fe+8/3 + 8e- ---- 3Fe0 1 окислитель, восстановление
C+2 - 2e- ---- C+4 4 восстановитель, окисление3Mn3O4 + 8Al ---- 9Mn + 4Al2O3
3Mn+8/3 +8e- ---- 3Mn0 3 окислитель, восстановление
Al0 - 3e- ---- Al+3 8 восстановитель, окисление
5.2. Задания для самостоятельной работы.
Методом электронного баланса подобрать коэффициенты в ОВР, указать окислитель, восстановитель и процессы окисления и восстановления.
а) KMnO4 + KI + H2SO4 = I2 +MnSO4 + K2SO4 + H2O
б) Cr(NO3)3 + NaBiO3 + HNO3 = H2Cr2O7 + Bi(NO3)3 + NaNO3 + H2O
в) NaBr + KMnO4 + H2O = Br2 + MnO2 + NaOH + KOH
г) CH2 = CH2 + KMnO4 + H2O = HO - CH2 - CH2 - OH + MnO2 + KOH
д) C6H12O6 + KMnO4 + H2SO4 = MnSO4 + K2SO4 + H2O + CO2
е) As2S3 + HNO3 + H2O = H3AsO4 + H2SO4 + NO
ж) Fe3O4 + CO = Fe + CO2
з) Mn3O4 + Al = Mn + Al2O3
и) Cu3O2 + HCl ---- Cu + Cl2 + H2O
к) C3H8O3 + O2 ---- CO2 + H2O