Конспект урока химии в 9-м классе по теме "Обобщение и повторение материала по теме «Подгруппа азота»"
Задачи урока: систематизировать сведения учащихся о свойствах элементов подгруппы азота и их соединений; закрепить полученные навыки по составлению уравнений реакций и решению расчетных задач.
ХОД УРОКА
- Здравствуйте, садитесь. Тема сегодняшнего урока - «Обобщение и повторение материала по теме« Подгруппа азота». Мы вспомним и систематизируем знания, полученные на предыдущих уроках. В начале
проведем фронтальный опрос с помощью карт, которые лежат у вас на партах, Будем обсуждать теоретическую часть и решим несколько цепочек превращений, в конце урока - cамостоятельная работа.
У вас на партах лежат технологические карты «Подгруппа азота». На доске - таблица для повторения.
Карта для обобщения, повторения и проверки полученных знаний по теме «Подгруппа азота»
Таблица V группы главной подгруппы (на доске)
| Хим. знак | Лат. название | Название | Степень окисления |
|
N |
Эн |
Азот | -3, 0, +2, +3, +4, +5 |
|
P |
Пэ |
Фосфор | -3, 0, +3, +5 |
|
As |
Арсеникум |
Мышьяк | 0, +3, +5 |
|
Sb |
Стибиум |
Сурьма | 0, +3, +5 |
|
Bi |
Висмут |
Висмут | 0,+3, +5 |
- Напишите символы элементов в первую таблицу карты. Сверим с доской.
I. Рассказ учителя
Азот в переводе «безжизненный». Азот - элемент 2-го периода V группы главной подгруппы периодической системы, порядковый номер 7, соответственно его электронная формула 1s2
2s2 2p3 .
Азот обладает высокой электроотрицательностью, третий после F и О.
Проявляет типичные неметаллические свойства.
Состоит из неполярных молекул с очень устойчивой ковалентной связью , его структурная формула N=N, чем объясняется химическая инертность при обычных условиях.
В лаборатории азот получают термическим разложением нитрита аммония:
t
NH4NO2 = N2+H20
Шкала степеней окисления азота (ученик у доски проставляет промежуточные степени окисления азота, остальные делают то же в своих картах).
| +5 | N2O5, NO3-, HNO3, NaNO3, AgNO3 |
| +4 | NO2 |
| +3 | N2O3, NO2-, HNO2, NaNO2, NF3 |
| +2 | NO |
| +1 | N2O |
| 0 | N2 |
| -3 | NH3, NH4+, NH4OH, NH4Cl, Li3N, Cl3N |
II. Работа учеников на карточках с проверкой у доски
(Возможно вызывать к доске по трое, остающиеся на местах ученики заполняют технологические карты)
1) Как изменяются металлические свойства в ряду:
N P As Sb Bi -> NH3
2) Расставьте степени окисления в молекуле аммиака: N-3 H3 +1
3) Физические свойства аммиака - бесцветный газ с резким запахом, основное свойство - растворимость в воде - 700 : 1
4) Напишите структурную формулу аммиака
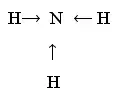
Пространственная структура - пирамида, в центре - N. Какой тип химической связи? (Ковалентная полярная)
5) Напишите структурную формулу катиона аммония - sp3-гибридизация

Пространственная структура - пирамида, валентный угол ~ 109,5
6) Важнейшее химическое свойство аммиака - взаимодействие с кислотами.
Закончите уравнения реакции взаимодействия аммиака с кислотами:
NH3 + HCl = NH4Cl
NH3 + H2SO4 = (NH4)2SO4
7) Как аммиак ведет себя в окислительно-восстановительных реакциях? Проставьте степени окисления и коэффициенты.
2N-3H3 + 3Cu+20 = 2Cu0 + 3H2O + N20
8) В лаборатории аммиак можно получить по реакции (закончите реакцию)
2NH4Cl + Ca(OH)2 = CaCl2 + 2NH3 + 2H2O
(тв.) (тв.)(г)
9) Качествна аммиак:
NH3 + HCl = NH4Cl
(г) (г) (тв.)
- Что наблюдаем? (Образование белого дыма)
III. Рассказ учителя
Концентрированная азотная кислота окисляет соляную кислоту, смесь этих кислот называется «царской водкой» - переводит в раствор золото и платину.
HNO3 + 3 HCl == NOCl + Cl2 + 2H2O
Au + HNO3 + 3HCl = Au Cl3 + NO + 2H2O
Азотная кислота - сильный окислитель, при взаимодействии с металлами только часть ее расходуется на образование соответствующей соли - нитрата, другая же выступает как окислитель, восстанавливаясь до NO2, NO, N2, NH3.
IV. Работа учеников на картах с проверкой у доски
1. Азотная кислота - сильная, полностью диссоциирует на ионы:
HNO3
H+ + NO3-
2. Азотная кислота - не стойкое соединение, разлагается уже при комнатной температуре
HNO3 --> O2 + NO2 + H2O
3. Взаимодействие HNO3 с металлами
3 Cu + 8HNO3 = 3Cu(NO3)2 + 2 NO + 4H2O Разб. HNO3
ок
N+5 +3e --> N+2 2
ок-ль в-е
CuО - 2e --> Cu + 2 3
в-ль
Cu + 4HNO3 = Cu(NO3)2+ NO2+ 2H2O
HNO3 взаимодействует с Al, Cr, Fe, Ni, пассивируя их
2Al + 6HNO3 = Al2O3 + 6 NO2 +3 H2O
4. Термическое разложение нитратов
| Металлы левее Mg | MeNO3 --> MeNO2 + O2
NaNO3 --> 2NaNO2 + O2 |
| Металлы от Mg до Cu | MeNO3 --> MeO + NO2 + O2
200оC Pb(NO3)2 --> 2PbO + 4NO2 + O2 |
| Металлы правее Cu | MeNO3 --> Me + NO2 + O2
300оC 2 AgNO3 --> 2Ag + 2NO2 + O2 |
5. Взаимодействие HNO3 с неметаллами
Концентрированная HNO3 окисляет неметаллы до высшей степени окисления:
P + 5 HNO3 = H3PO4 + 5 NO2 + H2O
S + 6 HNO3 = H2SO4 + 6 NO2 + 2H2O
(проставьте степени окисления)
Учитель обобщает, на доске рисует схему.

V. Фронтальная работа с классом
Учитель рассказывает, ученики заполняют соответствующие задания в карточках.
Фосфор - элемент 3-го периода V группы главной подгруппы периодической системы, порядковый номер 15, электронная формула фосфора: 1s2 2s2 2p6 3s2 3p3.
Шкала степеней окисления фосфора:
| +5 | P2O5, PO4 -3 , H3PO4, K3PO4, PCl5 |
| +3 | P2O3 |
| 0 | P (P4, Pn) |
| -3 | PH3 |
Аллотропия - образование одним и тем же химическим элементом различных веществ.
Красный фосфор - Pn - полимер, атомная кристаллическая решетка, входит в состав спичек, не ядовит.
240-400оC
Pn + O2 ----------- P2O5
Белый фосфор - P4 - схема строения молекулы:
t комн.
светится на воздухе: P4 +3O2 -------------- 2P2O3 + Q
ядовит
Фосфорная кислота - H3PO4 - трехосновная кислота (по 1 ступени средней силы, по 2-й и 3-й - слабой)
Диссоциирует ступенчато:
I. H3PO4 ==== H+ + H2PO4-
II. H2PO4- ==== H+ + HPO42-
III. HPO4- ==== H+ + PO43-
- Следовательно, возможно образование кислых солей.
Закончите уравнение реакции:
P2O5 + 3H2O = 2H3PO4
P2O5 + 3CaO = Ca3(PO4)2
P2O5 + 6NaOH = 2Na3PO4 + 3H2O
t
Ca3(PO4)2 + 3H2SO4 == 3CaSO4 + 2H3PO4
2H3PO4 + 3CaO = Ca3(PO4)2 + 3H2O
Первые три ученика, выполнившие задания, получают оценки.
Подготовленные, мотивированные классы успевают повторить свойства фосфора и сделать самостоятельную работу.
VI. Самостоятельная работа по карточкам (Приложение)
Всего четыре варианта по 5 реакций в каждом. Учитель раздает карточки, ученики начинают работать. Через 10 мин. работы собираются.
- Сдаем задания. Спасибо. До свидания.
VII. Подведение итогов
VIII. Домашнее задание: повторить § 38, задания 7, 8, 11 после параграфа.