Урок химии по теме «Металлы». 11-й класс
Тип урока: изучение и первичное закрепление новых знаний и способов деятельности.
Цели урока:
- Образовательная: учащиеся должны повторить известные сведения о строении атомов металлов, коррекция знаний учащихся характеризовать общие химические свойства, записывать уравнения химических реакций.
- Развивающая: создать условия для формирования умения анализировать
- информацию, выделять главное, существенное, продолжить развитие навыков самостоятельного умственного труда, умение сравнивать, наблюдать, делать выводы.
- Воспитательная: продолжить работу по воспитанию аккуратности, коммуникативности, взаимопомощи.
Средства обучения:
1) ПСХЭ Д.И.Менделеева,
2) раздаточный материал: таблица «Физические свойства металлов (Приложение 1);
3) демонстрационные таблицы: кристаллическая решетка металлов;
4) коллекция «Металлы и сплавы»;
5) модели кристаллических решеток металлов;
6) мультимедийный проектор.
Форма организации работы в классе: индивидуальная, фронтальная, парная.
ХОД УРОКА
1. Организационный момент (1 мин.)
(Настроить учащихся на активную, плодотворную работу.)
2. Постановка цели (2 мин.)
Учитель: Мы приступаем к изучению большой темы «Вещества и их свойства». Изучение веществ начинаем с самой многочисленной и разнообразной группы - металлов. Цель урока: обобщить систематизировать знания о Ме, которые вы получили при изучении химии в 8,9,10 классах и повседневной жизни. Записываем тему урока «Металлы». (Беседа с учащимися о значении металлов).
Учитель сообщаетплан урока (учащиеся записывают в тетрадях):
1. Хим. элементы металлы (Ме):
а) положение в ПСХЭ Д.И.Менделеева;
б) особенности электронного строения атомов.
2. Простые вещества Ме:
а) структура простых веществ, физические свойства;
б) общие химические свойства.
2. Актуализация опорных знаний (10 мин.)
Предварительный контроль: (учитель проводит фронтальный опрос)
Вопрос: Охарактеризуйте положение Ме в ПСХЭ Д.И.Менделеева.
Вопрос: Каковы особенности строения атомов химических элементов металлов?
Вопрос: К каким семействам относят элементы Ме?
Учитель: Рассмотрим строение атомов s,p,d-элементов Ме.
Учитель организует самостоятельную работу по группам. Карточка с заданием у каждого ученика на столе.
Задание: Запишите схемы строения атомов: натрия (1 группа), алюминия (2 группа), железа(3группа).
По одному человеку от каждой группы работают у доски, а остальные ученики - в рабочих тетрадях. Учащиеся записывают схемы строения атомов, электронные и электронно-графические формулы.
(Индивидуальный опрос: учитель проверяет работу учащихся у доски).
Самопроверка знаний: ученики оценили свою работу, обратили внимание на особенности строения d-элементов.
Учитель: Какие значения степеней окисления могут проявлять эти элементы?
Задание: Сравните число значений степеней окисления у элементов побочных подгрупп с элементами главных подгрупп. (Ученики отвечают на вопросы, указывая на большее значение степеней окисления у элементов побочных подгрупп, связывая это с большими валентными возможностями атомов).
3. Введение новых знаний (10 мин.)
Учитель: Какими свойствами обладают атомы Ме?
Задание: Дайте определение химическим элементам Ме исходя из особенностей строения их атомов. (Ученики отвечают на вопрос, дают определение химическим элементам Ме).
Учитель: Переходим к рассмотрению простых веществ Ме. На основании особого строения атомов у Ме - простых веществ существует особый вид связи.
Какой тип связи характерен для простых веществ Ме? (ученики отвечают на вопрос).
Металлическая связь - это связь в металлах и сплавах между катионами металлов, нейтральными атомами за счёт свободных электронов. ( Ученики записывают в тетради определение металлической
связи).
Учитель: (демонстрирует таблицу «Кристаллическая решетка металлов»).

Учитель: Раз у всех металлов одинаковый вид связи, то и тип кристаллической решётки, тоже одинаковый. Какой? Что находится в узлах кристаллической решётки металлов?
Чем они связаны? (Ученики отвечают на вопросы). Изображение кристаллической решетки условно, так как атом, теряя электрон, превращается в ион, а ион, присоединяя электрон, превращается в
атом. То есть система динамическая. Поскольку у металлов тип кристаллической решетки один, то и физические свойства металлов общие.
Учитель: (Демонстрирует образцы металлов).
Пользуясь таблицей «Физические свойства металлов», перечислите общие физические свойства металлов. (Ученики называют общие физические свойства Ме).
Учитель: Общие физические свойства металлов объясняются наличием свободных электронов. Однако у металлов, наряду с общими, есть и специфические физические свойства.
Задание: Используя таблицу «Физические свойства металлов», назовите металлы, которые обладают специфическими физическими свойствами. ( Ученики сравнивают физические свойства металлов, отмечают металлы с особыми свойства).
Учитель: Специфические физические свойства обусловлены, различными типами металлических кристаллических решеток. (Демонстрирует различные типы металлических кристаллических решёток).
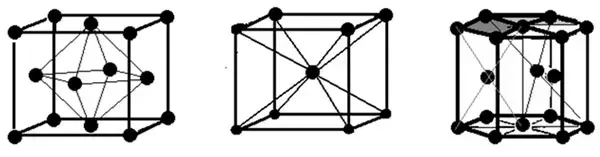
5. Первичное обобщение и ведение новых знаний в систему знаний учащихся. (15 мин.)
Учитель: Особое строение атомов, особый вид химических свойств, приводит к особым химическим свойствам металлов. В химических реакциях атомы металлов отдают электроны, превращаясь в положительно заряженные ионы:
Ме0 - ne --> Me+n (процесс окисления)
восстановитель
(Ученики записывают схему в тетради и делают вывод о восстановительных свойствах простых веществ металлов.)
Учитель: Познакомимся с химическими свойствами Ме. Рассмотрим взаимодействие Ме с простыми веществами. Демонстрирует опыты с помощью мультимедийного проектора: «Горение
железа кислороде»; «Взаимодействие железа с серой»;
«Взаимодействие сурьмы, меди и железа с хлором».
Задание: рассмотрите реакцию « Горение железа в хлоре» как окислительно-восстановительную. Текущий контроль: ученики записывают уравнение химической реакции,
указывают окислитель и восстановитель. Один ученик выполняет это задание на доске.
Обращаем внимание на значение степени окисления железа в этой реакции. Учащиеся прогнозируют состав продуктов реакций, степени окисления Ме в соединениях с серой.
Учитель: Рассмотрим взаимодействие Ме со сложными веществами. По степени активности металлы располагают в ряд напряжений, в котором металлы расположены в порядке убывания их восстановительных свойств и усиления окислительных свойств их ионов. Он характеризует активность металлов в ОВР, протекающих в водных растворах.
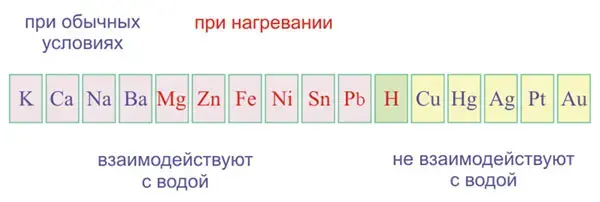
Демонстрирует опыты с помощью мультимедийного проектора:
«Взаимодействие натрия и кальция с водой», «Взаимодействие железа с серной кислотой», «Взаимодействие меди с раствором нитрата ртути (II)», «Взаимодействие натрия с этанолом».
Текущий контроль: ученики записывают уравнение одной из химических реакций, а остальные уравнения будут делать при выполнении домашнего задания. Один ученик выполняет это задание на доске,
рассматривает реакцию как окислительно-восстановительную, указывает окислитель и восстановитель. Ученики прогнозируют состав продуктов реакций, степени окисления Ме в образовавшихся
соединениях.
6. Закрепление и применение полученных знаний (2 мин.)
Учитель: Какие свойства проявляют в химических реакциях простые вещества металлы? (Ученики делают вывод о восстановительных свойствах простых веществ металлов).
7. Подведение итогов урока (2 мин.)
Учитель: Сегодня мы рассмотрели химические элементы и простые вещества металлы. Выяснили общие и специфические физические свойства простых веществ металлов. Рассмотрели общие
химические свойства простых веществ металлов. Ещё раз убедились в том, что свойства веществ зависят от строения. Что нового вы узнали о простых веществах Ме?
Учащиеся перечисляют, что нового узнали о металлах и оценивают свою работу на уроке. Учитель комментирует оценки и выставляет их в журнал.
8. Информация о домашнем задании (3 мин.)
§ №18.Написать уравнение наблюдаемых реакций и рассмотреть их, как ОВР:
- на оценку «5»: составить уравнение электронного баланса, указать окислитель и восстановитель, процессы окисления и восстановления для всех реакций;
- на оценку «4»: составить уравнение электронного баланса, указать окислитель и восстановитель, процессы окисления и восстановления для четырех реакций;
- на оценку «3»: составить уравнение электронного баланса, указать окислитель и восстановитель, процессы окисления и восстановления для двух реакций.
Задание индивидуальное: подготовьте сообщение о применение металлов, основанное на их особых свойствах.