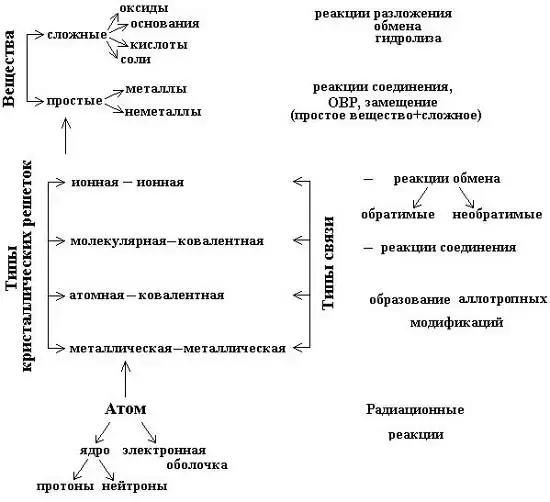
Строение вещества. Химические реакции (11-й класс)
Тип урока: урок обобщения и систематизации знаний и умений.
Форма урока: семинар - практикум
Цели урока:
- Повторить, углубить и обобщить сведения о строении веществ, химических реакциях и способах управления ими, практическое применение.
- Показать зависимость свойств веществ от химической связи и строения вещества.
- Охрана окружающей среды.
Дидактические цели:
знать:
- основные виды химической связи;
- типы кристаллических решеток в веществах с различным видом химической связи;
- причины многообразия органических соединений;
- понятие "электроотрицательность", "степень окисления", "ОВР";
- сущность реакции ионного обмена;
- признаки классификации химических реакций;
- понятия скорости химической реакции, катализатора, ингибитора;
- понятие гидролиза;
- типы химических реакций.
уметь:
- объяснить способы образования ионной, ковалентной, донорно-акцепторной, водородной связей;
- объяснить зависимость химических свойств органических веществ от вида химической связи и наличия функциональных групп;
- определить возможность образования водородной связи между молекулами органических веществ;
- определить тип кристаллической решетки в веществах с различным видом связи;
- определить принадлежность веществ к определенному классу веществ;
- характеризовать свойства веществ на основе их состава и строения;
- составлять химические уравнения ОВР;
- составлять полные и краткие уравнения реакций, разъяснять их смысл в свете ТЭД;
- давать характеристику заданной реакции;
- характеризовать изученные основные виды химических реакций между органическими веществами;
- объяснять сущность химических превращений, классифицировать предложенные химические реакции;
- объяснять действия факторов, влияющих на скорость реакций;
- на изученных примерах объяснять сущность гидролиза солей, записывать уравнения реакций гидролиза;
- определять тип химической реакции по всем известным признакам классификации.
1. Фронтальная работа с классом:
- Определение темы урока.
- Выяснение цели урока.
- Регламент работы секций.
- Выполнение заданий.
2. Обобщение знаний по теме "Строение вещества" (работа и сообщения по секциям)
План:
- "Строение вещества"
1. Строение атома. Изотопы. (Сообщение)
секция физиков
2. Кристаллические решетки и свойства веществ, зависящих от кристаллической решетки. (Сообщение)
секция экологов
3. Строение простых и сложных веществ. Виды связей. (Сообщение)
Лабораторный опыт: "Пространственное строение вещества" (модели органических и неорганических веществ)
секция химиков
4. Комплексные соединения. (Сообщение)
Лабораторный опыт:
4FeCl3+3K4[Fe(CN)6]->Fe4[Fe(CN)6] 3+12KCl
3FeSO4+2K3[Fe(CN)6]->Fe3[Fe(CN)6]2+3K2SO4
секция аграриев
5. Дисперсные системы. Эволюция коллоидных систем в процессе развития жизни на Земле. (Сообщение)
секция биологов
Строение белка, ДНК. (Сообщение)
Лабораторный опыт: Цветная реакция на белок, ксантопротеиновая реакция.
Белок + CuSO4 + NaOH - окрашивает фиолетово-красным
Белок + HNO3 (конц.) - желтое окрашивание
секция медиков
- Химические реакции их практическое применение
1. Характеристика химических реакций по изменению степени окисления и их практическое значение.
Влияние микроэлементов.
Секция медиков
2. Характеристика химических реакций по изменению степени окисления и их практическое значение.
По числу и составу реагирующих и образующихся веществ:
- разложения;
- соединения;
- замещения;
- обмена.
Секция химиков
3. Характеристика химических реакций по изменению степени окисления и их практическое значение.
По использованию катализатора:
- каталитические реакции;
- некаталитические реакции.
Опыт 1.
Н2О2 + катализатор
Н2О2 - без катализатора
Опыт 2. Действие Н2О2 на сырой и вареный картофель.
секция биологов
4. Характеристика химических реакций по изменению степени окисления и их практическое значение.
Реакции по направлению:
- обратимые;
- необратимые.
секция аграриев
5. Характеристика химических реакций по изменению степени окисления и их практическое значение.
Качественные реакции на вещества:
Лабораторный опыт: распознавание (качественные реакции на ионы). SO2-4, Cl-, NH+4, глюкоза, крахмал, глицерин.
секция экологов
6. Характеристика химических реакций по изменению степени окисления и их практическое значение.
7. По виду энергии, инициирующей реакцию:
- электрохимические;
- фотохимические;
- радиационные.
(Сообщение)
Лабораторный опыт: электролиз NaCl, CuCl2
секция физиков
- Подведение итогов:
-
- выступления;
- выполнение заданий;
- проведение опытов;
- составление опорных схем по выступлениям "Соответствие строения вещества - химические реакции" (от простого к сложному).