Презентация "Первоначальные химические понятия"
Скачать презентацию (5.37 МБ)
Объяснительная записка.
В 2006 году мною была опубликована программа пропедевтического курса химии для 7 класса. Для эффективного изучения теоретических первоначальных понятий химии детьми более раннего возраста предлагаю использовать на уроках презентацию, составленную по авторским разработкам, по опорным схемам-конспектам, разработанным на кафедре общей и аналитической химии МПГУ, материалам учебника "Химия-8" Г.Е. Рудзитиса, Ф.Г. Фельдмана; рабочей тетради для 8 класса "Первоначальные химические понятия" И.Н. Городничевой, рабочей тетради для 8 класса "Химические элементы и химические законы" И.А. Леенсона, рабочей тетради для 7 класса О.С. Габриеляна, Г.А. Шипаревой. Также данный материал можно использовать при изучении темы "Первоначальные химические понятия" в 8 классе и отдельные слайды презентации помогают актуализировать знания по отдельным темам на более высоких ступенях обучения химии.
Описание презентации с приемами использования отдельных ее слайдов на уроках. (Презентация)
Слайд 1. Титульный лист.
Слайд 2. Физическое тело и вещество.
Физические тела состоят из веществ. Ученикам предлагается выписать в два столбика физические тела и вещества из данного списка.
Слайд 3. Физическое тело и вещество.
После самостоятельной работы предлагается самопроверка получившихся результатов.
Слайд 4. Разделение смесей.
Представлены способы разделения смесей.
Слайд 5. Атомы и молекулы.
Физические тела состоят из веществ; вещества состоят из молекул, в состав которых входят атомы или из атомов, не связанных в молекулы.
Ученики под схемой выписывают из учебника определение понятий "молекула" и "атом".
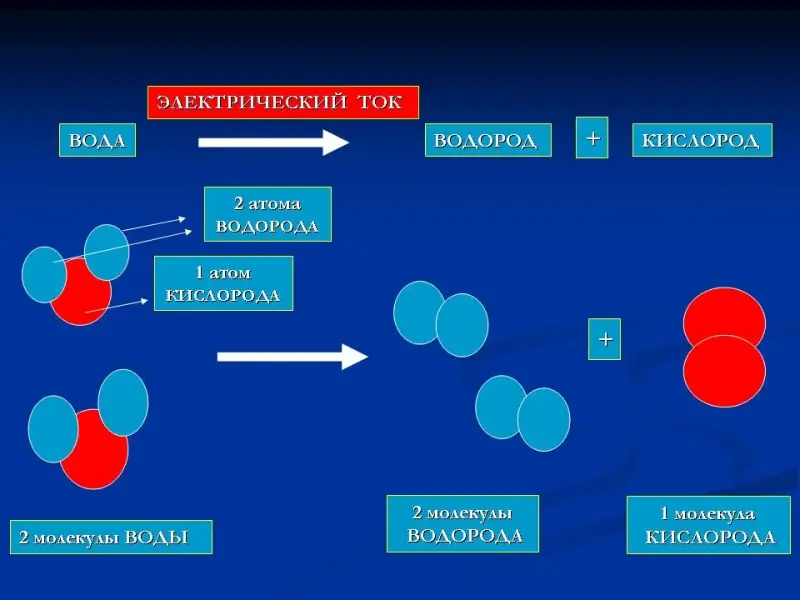
Слайд 6. Схема разложения воды электрическим током - опыт, подтверждающий наличие молекул и атомов.
Слайд 7. Атомно-молекулярное учение М.В.Ломоносова.
Ученикам предлагается расшифровать опорный конспект:
- Молекулы состоят из атомов.
- Вещества бываю молекулярного (т.е. состоят из молекул) и немолекулярного строения (состоят из атомов, несоединенных в молекулы).
- Молекулы находятся в непрерывном движении. Между молекулами действуют силы взаимного притяжения и отталкивания.
- Атомы одного вида от атомов другого вида отличаются массой и свойствами.
- Между молекулами существуют промежутки, которые зависят от температуры и агрегатного состояния вещества.
- С веществами могут происходить физические и химические явления. При физических явлениях молекулы не изменяются, меняется расстояние между ними. При химических явлениях молекулы распадаются до атомов и атомы образуют новые комбинации молекул.
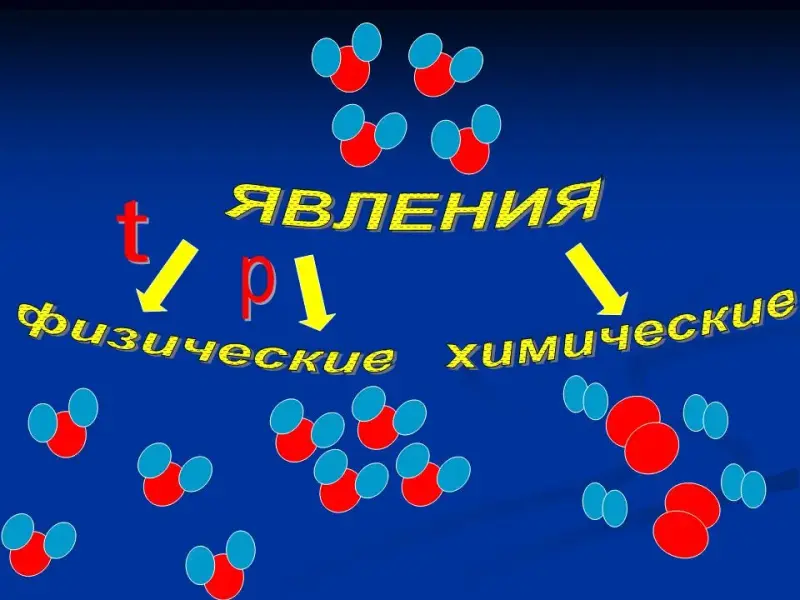
Слайд 8. Химические и физические явления.
Под схемой учащиеся записывают определение явлений и примеры.
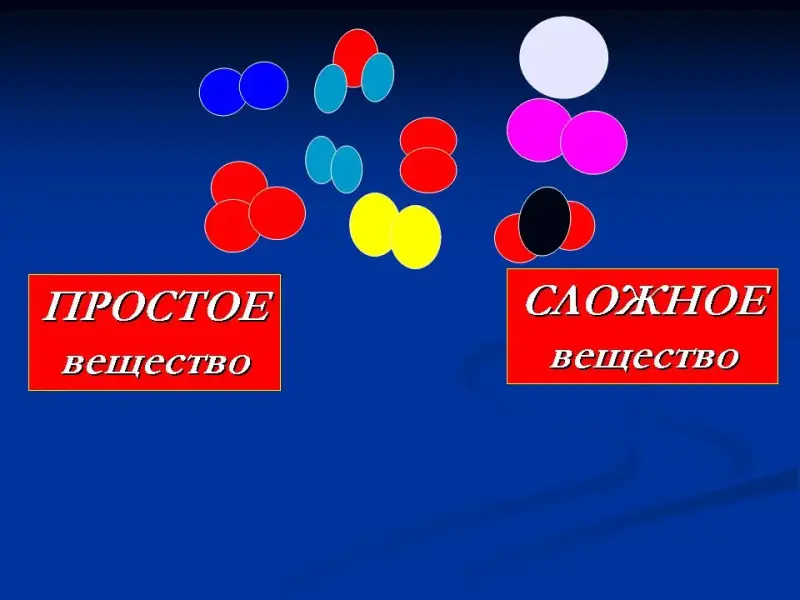
Слайд 9. Простые и сложные вещества.
В два столбика ученики записывают определения понятий "простое вещество" и "сложное вещество", самостоятельно зарисовывают молекулы простых и сложных веществ из данного списка, распределяя их в соответствующие столбцы, затем проводиться самопроверка.
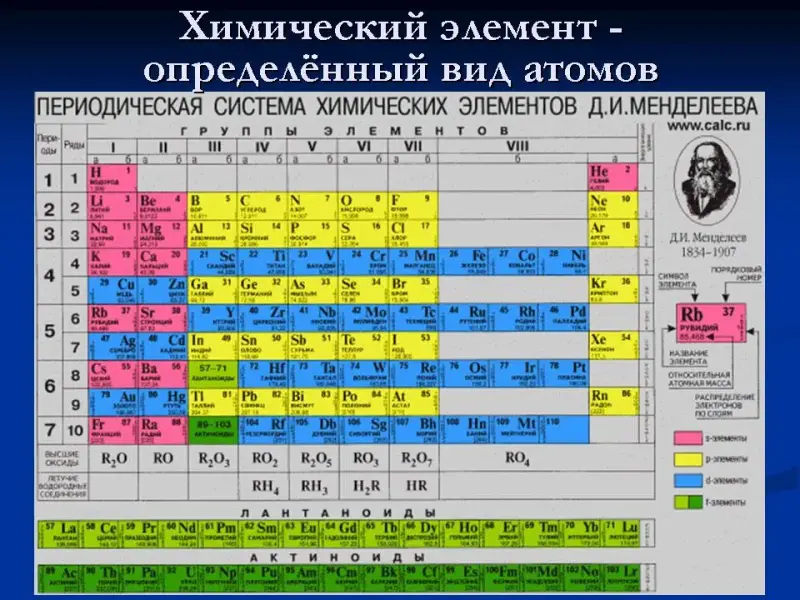
Слайд 10. Химический элемен.
Записывается определение. Знакомим с таблицей химических элементов Д.И.Менделеева.
Слайд 11. Алхимические символы химических элементов.
Знакомство и обсуждение записи химических элементов до XIX века.
Слайд 12. Обозначение химических элементов Берцелиусом.
Обсуждение современной системы обозначения химических элементов. Зарисовывается таблица с примерами, далее можно таблицу продолжить (без латинских названий) наиболее часто встречаемыми химическими элементами, пользуясь таблицей №2 учебника (стр. 24).
Слайд 13-14. Химические анаграммы.
Ученики устно отгадывают зашифрованные химические элементы.
Слайд 15. Химический диктант.
На слайде по вариантам записаны названия химических элементов. Учащимся предлагается записать знак химического элемента и чтение этого знака в формулах.
После написания диктанта возможна самопроверка или взаимопроверка работы.
Слайд 16-17. Химические элементы в организме человека.
Работа с таблицей макро-, микро- и ультра микроэлементов. Учащиеся выполняют задание на карточках (Приложение 1), выписывают знаки химических элементов.
Слайд 18. Атомная единица массы
Знакомство с новой единицей массы атома, образно показано чему равна 1 а.е.м. Ученики делают рисунки, записывают определение.
Слайд 19. Относительная атомная масса.
Знакомство с новой величиной, показано как выводится относительная атомная масса, обсуждение почему эта величина безразмерная. Образно показана относительная атомная масса гелия. Обсуждаем и записываем определение, ученики выполняют рисунок и правильно записывают массу атома гелия, выраженную в а.е.м. и относительную атомную массу гелия.
Слайд 20. Относительная атомная масса.
Учим находить относительную атомную массу химических элементов в периодической системе Д.И.Менделеева на примере водорода, кислорода, меди, записывать округленные значения величины. Далее ребята записывают относительные атомные массы различных химических элементов и массы атомов, выраженных в а.е.м. этих же элементов.
Слайд 21. Относительная атомная масса.
Обобщение знаний об относительной атомной массе оформляем в виде схемы.
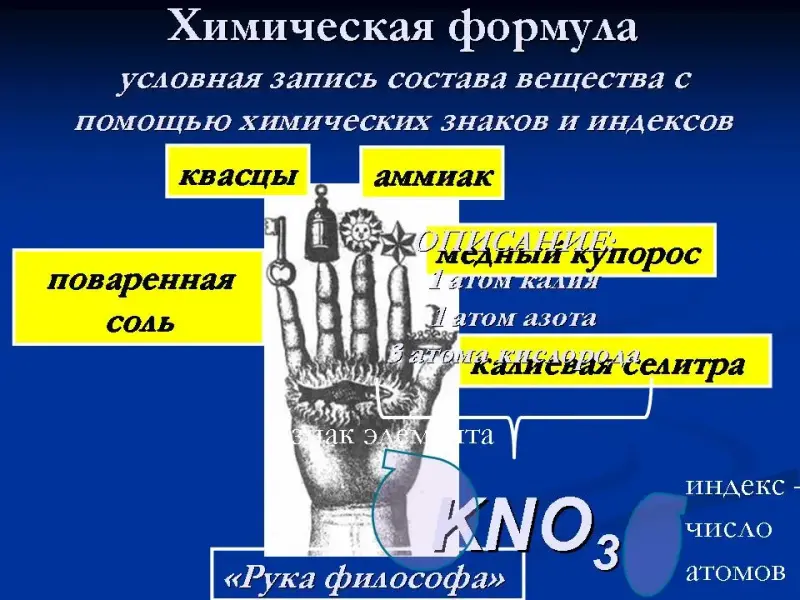
Слайд 22. Химическая формула.
Рассматривая три формы записи состава вещества: алхимическое изображение вещества, описание состава и химическую формулу с помощью знаков и индексов приводим учеников к выводу, что именно современная химическая формула, являясь емкой, отражает состав вещества. Записываем пример калийной селитры: описание и химическую формулу, формулируем и записываем определение понятия "химическая формула".
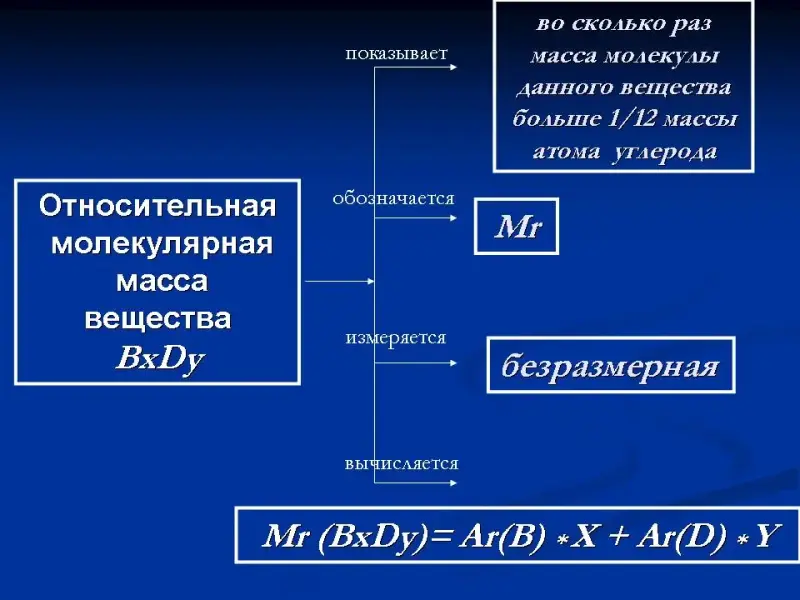
Слайд 23. Относительная молекулярная масса.
Схема-обобщение знаний об относительной молекулярной массе вещества.
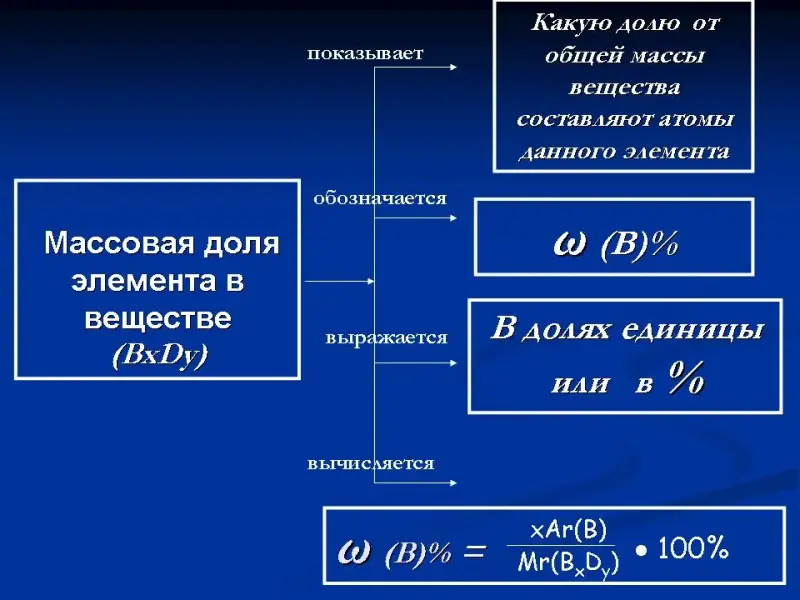
Слайд 24. Массовая доля элемента в веществе.
Схема-обобщение знаний о массовой доле элемента в веществе
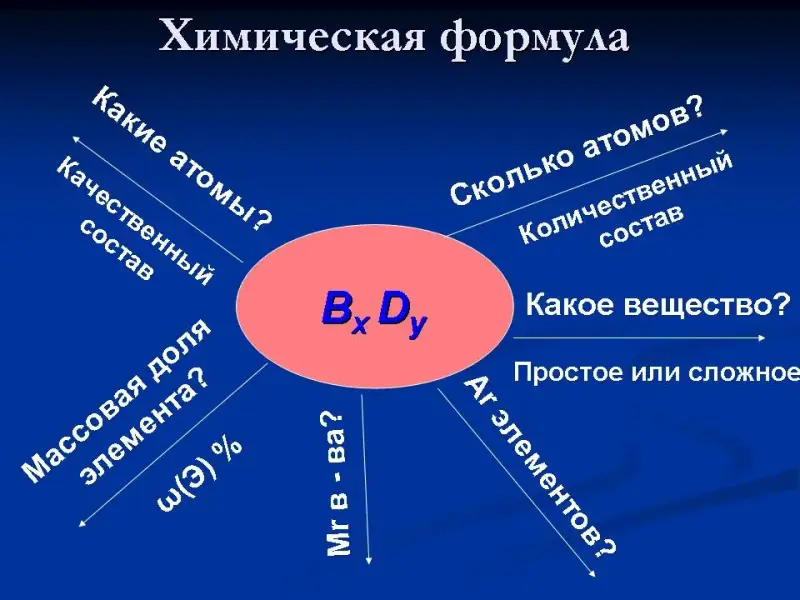
Слайд 25. Схема-обобщение "Химическая формула вещества".
Схема является ответом на вопрос учителя: "Какую информацию о веществе несет его химическая формула?" Относительные атомные массы элементов, входящих в состав данного вещества выписываются из периодической системы Д.И. Менделеева для дальнейшего подсчета относительной молекулярной массы вещества и определения массовых долей элементов, а так же с целью многократного повторения и выработки навыка правильной записи этой величины.
Слайд 26. Пример характеристики химической формулы углекислого газа.
Слайд 27-30. Алгоритм определения валентности по химической формуле вещества.
Представлены поэтапные действия для определения валентностей элементов в бинарных соединениях по молекулярной формуле вещества. Выводим с учениками обобщенную формулу для подсчета валентности элемента.
Слайд 31-35. Алгоритм составления химической формулы бинарного соединения по известным валентностям.
Рассматриваем и записываем поэтапно действия для составления молекулярной формулы вещества по валентностям. Выводим формулу для подсчетов индексов элементов.
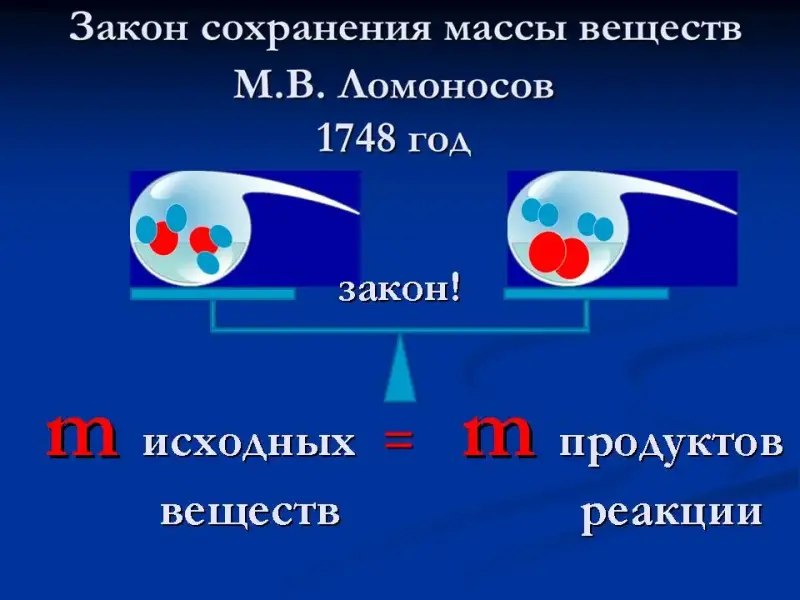
Слайд 36-37. Закон сохранения массы веществ М.В. Ломоносова.
Обсуждаем закон, ученики зарисовывают опорный сигнал, дают формулировку закона. Показываем фрагмент из кинофильма "Михайло Ломоносов" (1955 год), демонстрирующий публичный опыт М.В. Ломоносова.
Слайд 38-39. Уравнения химических реакций.
Записываем уравнение химической реакции разложения воды электрическим током. Вспоминаем формулировку закона сохранения массы веществ, подсчитываем массы исходных веществ и продуктов реакции и приходим к выводу, о необходимости расстановки коэффициентов, уравнивающих число атомов элементов до и после реакции. Ученики расставляют коэффициенты, записывают со слайда №38 расчет массы веществ с учетом коэффициентов, подтверждая соблюдение закона сохранения массы веществ. Формулируем определение уравнения химической реакции.
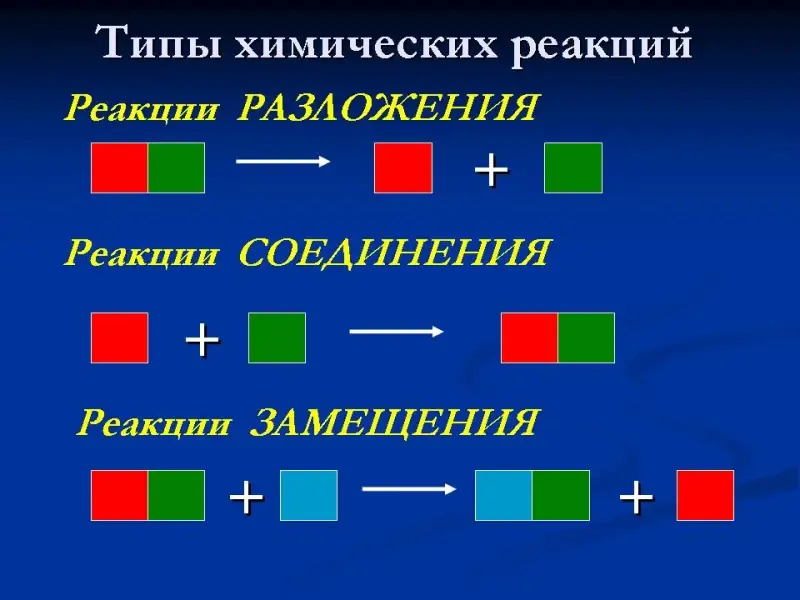
Слайд 40-41. Типы химических реакций.
Изучая типы химических реакций, зарисовываем схемы реакций разложения, соединения, замещения. Записываем уравнения реакций, соответствующие схемам, расставляем коэффициенты.
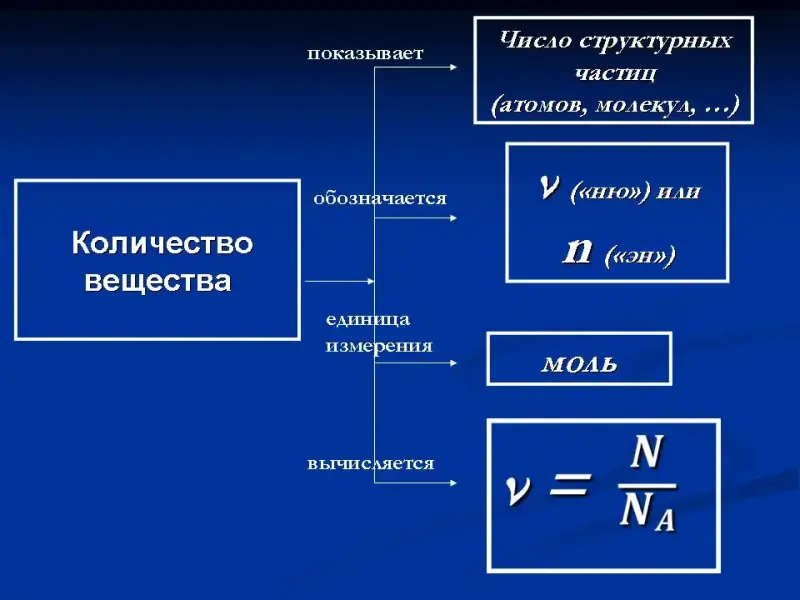
Слайд 42. Количество вещества.
Знакомство с новой физической величиной, иллюстрируем порцию вещества, записываем определение количества вещества, вводим обозначение n ("ню").
Слайд 43. Моль вещества.
Вводим понятия "моль вещества", "число Авогадро".
Слайд 44. Количество вещества.
Схема-обобщение знаний о количестве вещества.
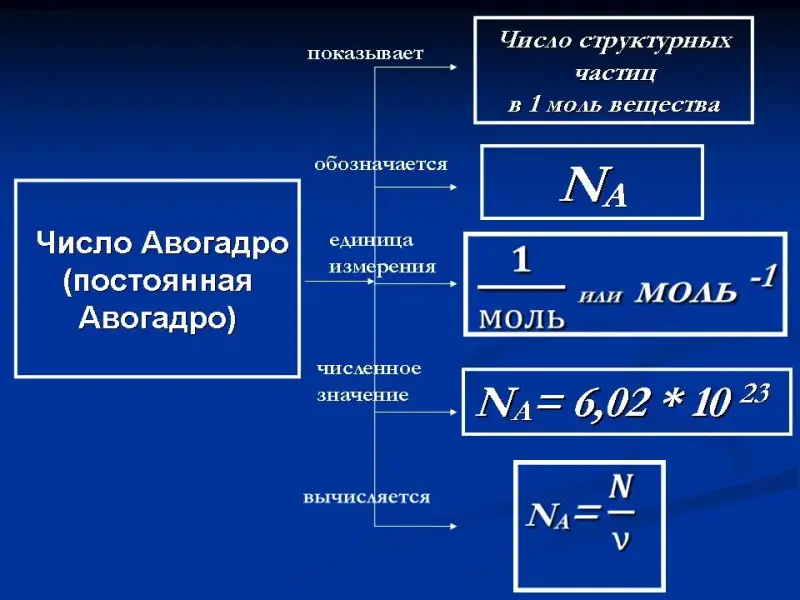
Слайд 45. Число Авогадро.
Схема-обобщение знаний о постоянной Авогадро.
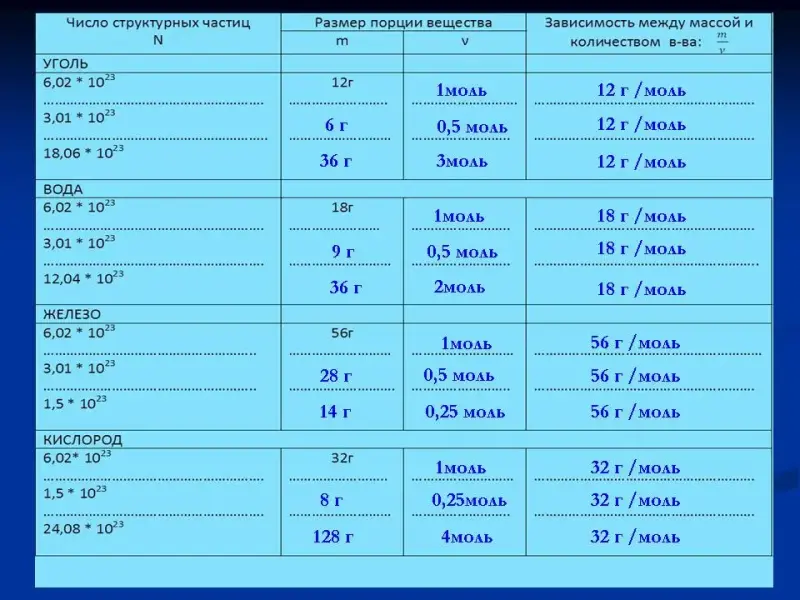
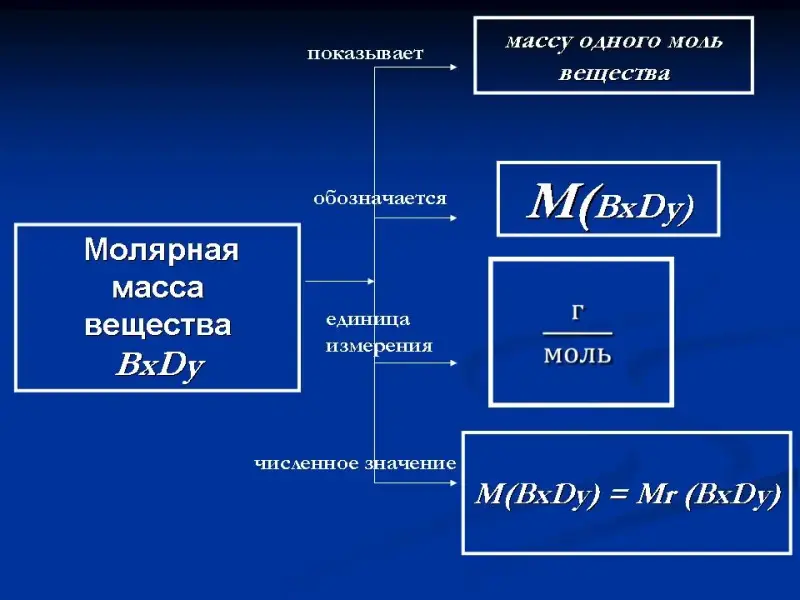
Слайд 46. Молярная масса.
Знакомство с новой физической величиной. Работаем с таблицей (Приложение 2), определяем зависимость между массой и количеством вещества для разных порций веществ. Знакомим с новой физической величиной, вводим обозначение, формулу для вычисления молярной массы, единицы измерения. Подводим учеников к выводу о численном равенстве относительной молекулярной массы и молярной массы данного вещества.
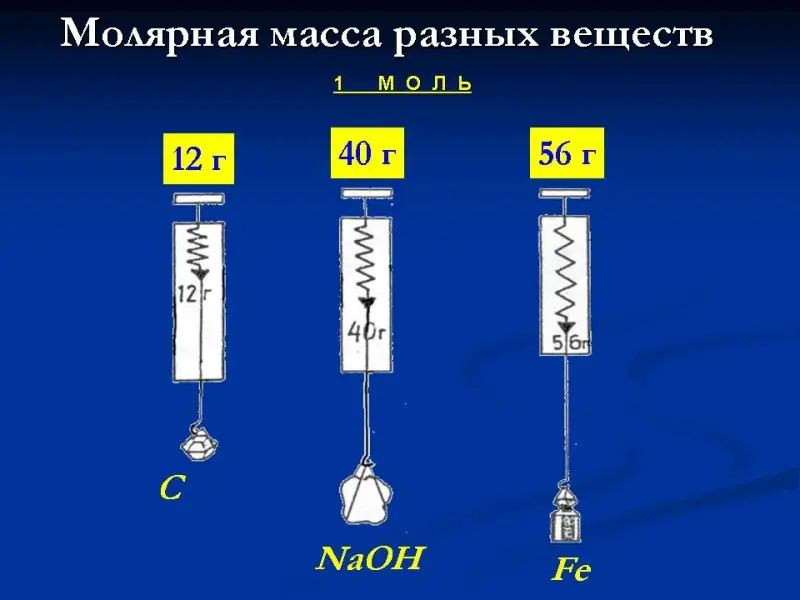
Слайд 47. Молярная масса разных веществ.
Рисунок закрепляет понимание о том, что у разных по составу веществ различны и молярные массы, хотя в них содержится одинаковое число частиц.
Слайд 48. Молярная масса.
Схема-обобщение знаний о молярной массе вещества.
Слайд 49. Закон Авогадро.
Записываем формулировку закона, рассматриваем и обсуждаем рисунок, изображающий 1 моль разных газов.
Слайд 50. Молярный объем.
Формируем понятие "молярный объем газов", рассматривая рисунок подводим к выводу, что для веществ в твердых и жидких агрегатных состояниях молярный объем различен, а в газообразном состоянии эта величина постоянна. Вводим размерность и формулу для вычисления.
Слайд 51. Молярный объем.
Схема-обобщение знаний о молярном объеме газов.
Слайд 52. Связь количественных величин.
Демонстрируем и обсуждаем сводную формулу взаимосвязи между физическими величинами: массой, объемом и числом структурных частиц, осуществляемой через количество вещества. Делаем вывод, что формула позволяет рассчитать любую из переменных величин, если известна лишь одна из них.
Слайд 53. Список литературы.