Предлагается разработка урока по теме “Окислительно-восстановительные реакции” для обучающихся 8-х классов. Приоритет разработки данной темы в том, что с небольшими изменениями (с учетом специфики учебного заведения и способностями учащихся) ее можно использовать учителям, работающим по разным учебникам и разным программам, так как она очень актуальна. Представлена презентация к уроку и распечатка маршрутного листа для обучающихся.
Проблемная тема урока: “Кто-то теряет, а кто-то находит”.
Цели урока:
формирование общеучебных умений и навыков, носящих в современных условиях общенаучный и общеинтеллектуальный характер;
развитие у обучающихся теоретического, творческого, логического и операционного мышления.
Задачи урока:
1) Учебная – расширить и закрепить:
– знания обучающихся о свойствах
металлов и неметаллов, типах химических реакций;
– умения показывать электронные переходы в ОВР,
определять значение степени окисления
химических элементов;
– навыки составления электронного баланса и
расстановки коэффициентов в уравнениях
окислительно-восстановительных реакциях.
2) Воспитательная – воспитывать чувство патриотизма.
3) Развивающая – расширение кругозора обучающихся, развитие умений и навыков применения полученных знаний для объяснения явлений окружающего мира.
Ход урока
I. Организационный момент
II. Введение в тему
Летом 2007 года в Европе были подведены итоги конкурса "Семь новых чудес света". Голосование проходило по Интернету, и отдать свой голос "за чудо" мог каждый желающий. Можно только догадываться, почему в список победителей не вошел ни один российский памятник, даже московский собор Василия Блаженного.
Газета "Известия", телеканал "Россия" и радиостанция "Маяк" выдвинули инициативу дать свой ответ "Семи новым чудесам света". Цель проекта “Семь чудес России” – возрождение чувства патриотизма и любви к своему Отечеству, а также привлечение внимания к восстановлению и сохранению исторических, культурных и природных объектов на территории нашей Родины. Итоги голосования по долгосрочному федеральному общероссийскому проекту были объявлены во время праздничного концерта на Красной площади по случаю Дня России. К “Чудесам” России относятся:
Долина гейзеров на Камчатке, озеро Байкал, дворцовый комплекс Петергоф под Санкт-Петербургом, природный памятник “Столбы выветривания” в Коми, собор Василия Блаженного в Москве, Мамаев курган и статуя Родины-матери в Волгограде, гора Эльбрус.
Результатом проекта стало составление нового “Золотого маршрута по России”, по которому, при желании, вы можете отправиться в путешествие.
Воображение правит миром
Наполеон 1
А если бы объявили конкурс “Семь чудес науки химии”? Какое, всем вам известное вещество возглавило бы список претендентов?
– Конечно же, вода. Я нисколько не сомневаюсь, что вы приведете массу доказательств того, что это удивительное вещество достойно первого места в списке. А вот на второе место я бы поставила окислительно-восстановительные процессы. Почему? На этот вопрос мы и постараемся ответить с вами в процессе урока.
Тема нашего урока: “Окислительно-восстановительные реакции”
III. Основная часть урока. Формирование новых знаний
Представьте себе, что Вы стоите перед домом, где живут удивительные существа (Ме, НеМе). Каждый житель имеет свою квартиру, живет на определенном этаже и в определенном подъезде. Представители высшего общества занимают элитный 8 подъезд, они держатся особняком, в контакты ни с кем не вступают и очень самодостаточны (Почему?). Все остальные жители очень хотят быть похожими на них. Для этого одни отдают, а другие принимают электроны. В этом случае атомы превращаются в ионы, которые имеют такую же электронную конфигурацию, как ближайшие к ним инертные газы.
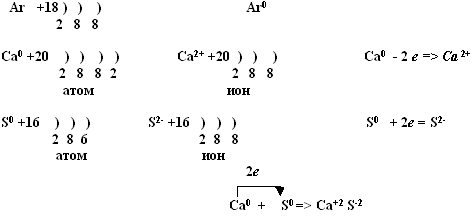
Электрон давно завоевал физику и химию, став для них почти что идолом. Все окислительно-восстановительные реакции находятся во власти электронных переходов от одного атома к другому как внутри молекулы, так и между ними. Перемещение электронов сопровождается изменением степени окисления атомов, участвующих в этих процессах.
Просмотр творческой работы обучающегося и его комментарии к ней:
Свойство металлов – отдавать электроны: у магния на последнем энергетическом уровне два электрона, которые он легко отдает, превращаясь в положительно заряженный ион. Свойство неметаллов – присоединять электроны: у серы на последнем энергетическом уровне 6 электронов, до завершения уровня не хватает двух электронов, которые она присоединяет, образуя анион.
Просмотр творческой работы обучающегося и его комментарии к ней:
“Окислитель, как грабитель, забирает электрон”. Хлор более сильный окислитель, чем сера, поэтому при взаимодействии железа с хлором образуется хлорид железа (+3)
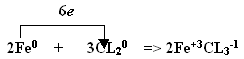
Вторая тема нашего урока: “Кто-то теряет, а кто-то находит”. (Почему?)
ОВР – это такие реакции, при которых происходит переход электронов от одних атомов, ионов или молекул к другим.
Окисление – это процесс отдачи электронов, степень окисления при этом повышается.
Восстановление – это процесс присоединения электронов, степень окисления при этом понижается.
Атомы, молекулы или ионы, отдающие электроны, являются восстановителями.
Атомы, молекулы или ионы, присоединяющие электроны, называются окислителями.
Окисление всегда сопровождается восстановлением, а восстановление окислением.
ОВР – это единство двух противоположных процессов: окисления и восстановления.
IV. Закрепление полученных знаний
1. Покажите электронные переходы в следующих ОВР.
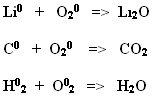
2. Назовите окислитель и восстановитель.
V. Расширение и развитие полученных знаний
Во многих ОВР очень трудно расставить коэффициенты, для этого используют метод электронного баланса, который основан на сравнении степеней окисления в исходных и конечных веществах.
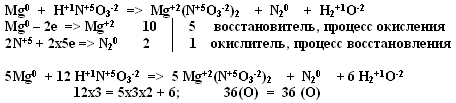
VI. Закрепление знаний
1. Из приведенных схем выпишите уравнения реакций, которые можно отнести к ОВР
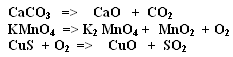
2. Расставьте коэффициенты методом электронного баланса в следующих схемах ОВР
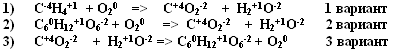
Определите окислитель, восстановитель, процесс окисления и восстановления.
3. Проверка выполнения задания (2)с помощью интерактивной доски (функция “штора”), или презентации
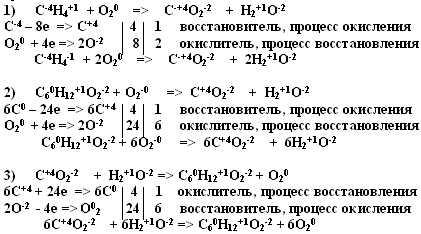
VII. Значение и применение ОВР
Вопросы к учащимся:
– Какой процесс отражает первое уравнение реакции?
– Какое значение имеют реакции горения?
– Какой процесс отражает второе уравнение реакции?
Первый вдох новорожденного говорит о начале новой жизни.
– Каковы функции дыхания?
Дыхание — основная форма диссимиляции у человека, животных, растений и многих микроорганизмов. При дыхании богатые энергией вещества, принадлежащие организму, полностью разлагаются до бедных энергией неорганических конечных продуктов (диоксида углерода и воды), используя для этого молекулярный кислород. Под внешним дыханием понимают газообмен между организмом и окружающей средой, включающий поглощение кислорода и выделение углекислого газа, а также транспорт этих газов внутри организма.
– Какой процесс отражает третье уравнение реакции?
– Какова функция фотосинтеза. Его значение?
Фотосинтез – процесс образования органических веществ из углекислого газа и воды на свету в зеленых листьях. Фотосинтез, является одним из самых распространенных процессов на Земле, он обуславливает природные круговороты углерода, кислорода и других элементов и обеспечивает материальную и энергетическую основу жизни на нашей планете. Фотосинтез является единственным источником атмосферного кислорода. К тому же фотосинтез снабжает человечество топливом (древесина, уголь, нефть), волокнами (целлюлоза) и бесчисленными полезными химическими соединениями. Процесс фотосинтеза является также основой питания всех живых существ, так как связанный из воздуха в процессе фотосинтеза углекислый газ и вода, образуют около 90-95% сухого веса урожая. Остальные 5-10% приходятся на минеральные соли и азот, полученные из почвы.
Как вы считаете, возможно, ли было возникновение жизни на нашей планете без участия окислительно-восстановительных процессов?
Поведение итогов
Итак, приступаем к голосованию. Кто считает окислительно-восстановительные процессы, в основе которых лежат электронные переходы, “чудом” науки? Кто не согласен? Кто сомневается? Обсудить.
VIII. Домашнее задание
- §17, §43.
- Творческое задание обучающимся. Рабочая тема “Семь аргументов в пользу “чуда””.
- Предложите на звание “чуда” примеры из цикла наук предметов естественнонаучного цикла.