Тип урока: комбинированный урок.
Цель урока: Повторить и систематизировать сведения об основных способах получения металлов в промышленности.
Задачи урока:
ОБУЧАЮЩИЕ
- обеспечить усвоение понятий об основных способах получения металлов: пирометаллургии, гидрометаллургии и электрометаллургии;
- Рассмотреть и сравнить различные способы получения металлов из природного сырья.
- Рассмотреть сущность электролиза, особенности электролиза растворов электролитов.
- Закрепить умение составлять окислительно-восстановительные реакции.
РАЗВИВАЮЩИЕ
- развивать умение логически мыслить,
- анализировать, делать обобщения и выводы,
- проводить сравнения;
ВОСПИТЫВАЮЩИЕ
- воспитывать умение находить главное,
- способствовать развитию интереса к учебе.
Оборудование: На столах учащихся:
- раздаточный дидактический материал;
- мультимедиопроектор;
- презентация.
Ход урока
I. Организационный момент.
1. Объявление темы и целей урока.
II. Повторение изученного материала.
Проведение самостоятельной работы
III. Изучение нового материала.
1. Металлы в природе. Металлургия.
Только в свободном виде встречаются золото и платина. И в самородном виде, и в форме соединений могут находиться в природе серебро, медь, ртуть и олово. Все остальные металлы, которые находятся в ряду напряжения до Sn, встречаются в природе только в виде соединений.
Среди таких соединений:
- хлориды (сильвин, галит, или каменная соль, сильвинит);
- нитраты (чилийская селитра);
- сульфаты (глауберова соль, гипс);
- карбонаты (мел, мрамор, известняк; магнезит, доломит);
- силикаты, в том числе содержащие алюминий – алюмосиликаты (белая глина, или каолин, полевые шпаты, слюда);
- сульфиды (серный колчедан, киноварь, цинковая обманка);
- фосфаты.
Минералы и горные породы, содержащие металлы или их соединения и пригодные для промышленного получения металлов, называются рудами.
Если руды содержат соединения двух или нескольких металлов, то они называются полиметаллическими. Например, медно-молибденовые, свинцово-серебрянные и т. д.
Металлургия – это отрасль промышленности, которая занимается получением металлов из руд. Так же называется и наука о промышленных способах получения металлов из руд.
2. Общие способы получения металлов.
1) Пирометаллургия – восстановление металлов из руд при высоких температурах с помощью восстановителей (углерода, оксида углерода (II), водорода, металлов – алюминия, магния).
Показ видеосюжета – получение меди из его оксида с помощью восстановителя – водорода.
Напишите уравнение этой реакции.
Показ видеосюжета – получение свинца из его оксида с помощью восстановителя угля.
Напишите уравнение этой реакции.
Показ видеосюжета – получение хрома алюмотермией.
Напишите уравнение этой реакции.
2) Гидрометаллургия - восстановление более активными металлами менее активных из растворов их солей.
Это получение металлов, которое проходит в два этапа:
- Природное соединение «растворяют» в подходящем реагенте с целью получения раствора соли этого металла.
- Из образовавшегося раствора данный металл вытесняют более активным металлом или восстанавливают электролизом.
Например, для получения меди из руды, содержащей оксид меди (II) CuO:
СuO + H2SO4 = CuSO4+ H2O
CuSO4+ Fe = FeSO4+ Cu
Таким же способом получают серебро, цинк, молибден, золото, уран и т. д.
3) Электрометаллургия - это способы получения металлов с помощью электрического тока (электролиза).
Давайте вспомним, что такое: электролиз, электролит, электрод, катод, анод, катионы, анионы.
При электролизе окислителем и восстановителем является электрический ток.
Процессы окисления и восстановления разделены в пространстве, они совершаются не при контакте частиц друг с другом, а при соприкосновении с электродами электрической цепи.
3. Электролиз водных растворов электролитьв.
Катодные процессы в водных растворах электролитов : катионы или молекулы воды принимают электронов и восстанавливаются.
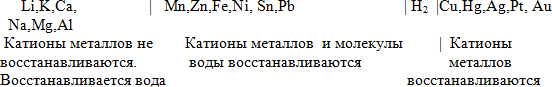
1. Катионы металлов со стандартным электродным потенциалом, большим, чем у ВОДОРОДА, расположены в ряду напряжений после него: Cu2+, Hg2+, Ag+, Pt2+, ..., до Pt4+. При электролизе они почти полностью восстанавливаются на катоде и выделяются в виде металла.
2H2O + 2e- = H2 + 2OH-
2. Катионы металлов с малой величиной стандартного электродного потенциала (катионы металлов начала ряда напряжений Li+, Na+, K+, Rb+, ..., до Al3+ включительно). При электролизе на катоде они не восстанавливаются, вместо них восстанавливаются молекулы воды.
2H2O + 2e- = H2 + 2OH-
3. Катионы металлов со стандартным электродным потенциалом меньшим, чем у ВОДОРОДА, но большим, чем у алюминия (Mn2+, Zn2+, Cr3+, Fe2+, ..., до H). При электролизе эти катионы, характеризующиеся средними величинами электроноакцепторной способности, на катоде восстанавливаются одновременно с молекулами воды.
Zn 2+ + 2e = Zn0
2H2O + 2e- = H2 + 2OH-
Рассмотрим электролиз расплава и раствора хлорида натрия.
Посмотрим видеофрагмент - электролиз раствора хлорида меди (II).
Напишите уравнение этой реакции.
IV. Закрепление.
- Что будет выделяться на катоде и аноде при электролизе растворов: нитрата серебра, сульфата натрия, бромида калия?
- Тестовая работа eor.edu.ru/card/624/testy-po-teme-metally-v-prirode-obshie-sposoby-ih-polucheniya.html
V. Итоги урока.
VI. Домашнее задание.
- § 18, стр. 214-222
- Повторить § 18, стр. 190-214
- Упр. 23, 28 стр. 225
VII. Оценки за урок.
VIII. Релаксация.
Литература и информационные ресурсы: eor.edu.ru/card/624/testy-po-teme-metally-v-prirode-obshie-sposoby-ih-polucheniya.html