Ход урока
I. Организационный момент:
а) приветствие;
б) объявление темы урока, запись в тетрадь;
в) основные учебные, воспитательные задачи урока.
Итак, ребята, ваш трудовой учебный день продолжается уроком химии, на котором вы познакомитесь с основными соединениями алюминия и их применением.
Основные задачи урока: усвоить основные соединения алюминия, познакомиться с их свойствами, закрепить понятие “амфотерность”, практические навыки при выполнении лабораторной работы, повторить правила по технике безопасности при работе с растворами кислот, щелочей, прививать экономное расходование реактивов.
Опрос пройденного материала в форме “деловой игры”.
а) группа “Поиск” (3 человека)
Задание: используя имеющуюся в классе
литературу, подготовить краткое сообщение о
применении алюминия.
б) группа “Экспериментатор” (2
человека)
Задание: из имеющихся реактивов получить
гидроксид алюминия. Составить схему превращений,
написать уравнения химических реакций с
пояснениями, т. е. в ОВР или ТЭД.
в) группа “Экономист-расчетчик” (2
человека)
К вам на предприятие поступил хлорид алюминия, из
которого получают алюминий. Химики-лаборанты
установили, что данная партия содержит 0,2
массовых долей примесей. Составить задачу и
рассчитать, сколько данного сырья необходимо
взять для получения 30 кг алюминия? Указать способ
получения алюминия”.
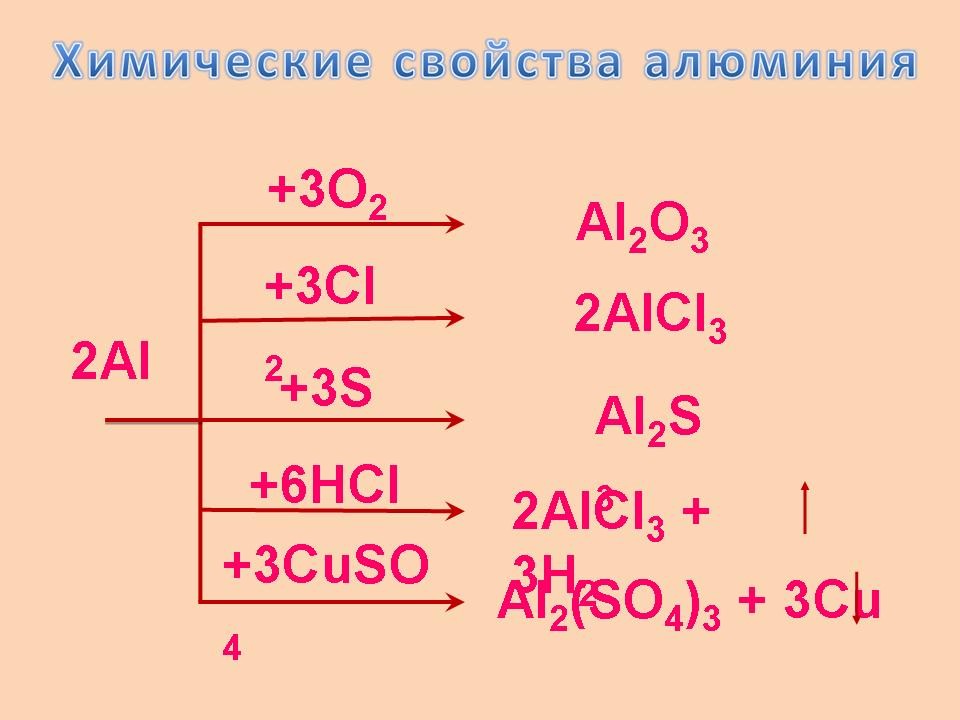
г) Ответ у доски-схемы;
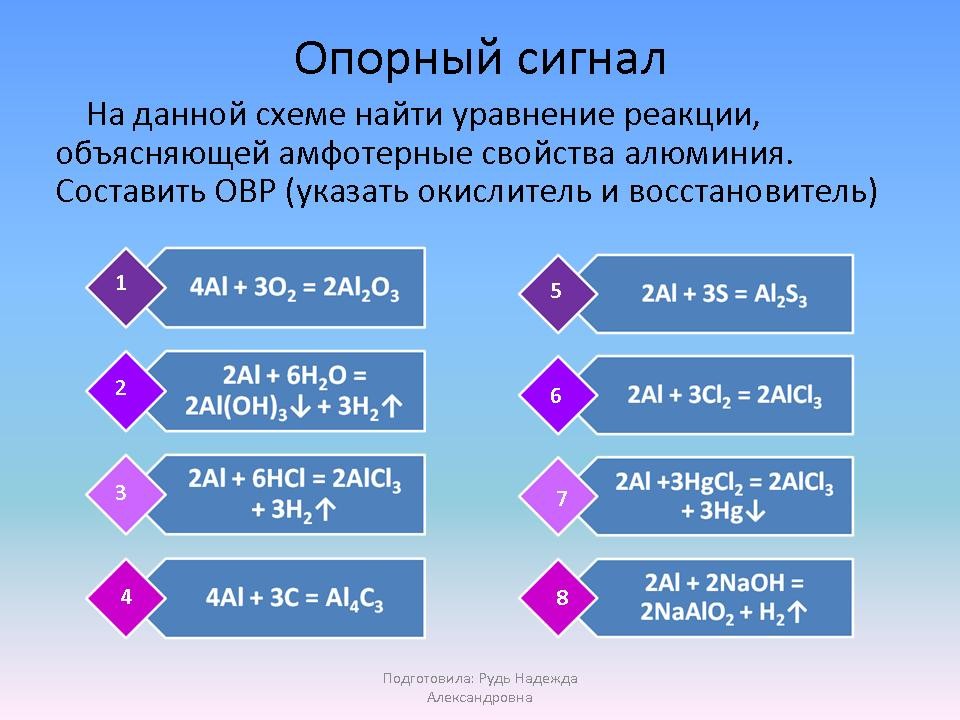
д) ответ по схеме “опорный сигнал”;
е) задание всему классу, а один ученик выполняет у
доски-раскладушки, а затем сверяют:
алюминий–>соль
алюминия–>алюминий–>гидроксид
алюминия–>оксид алюминия.
Используя формулы указанных соединений, а также условия протекания предложенных реакций.
Ответы учащихся.
1. Приложение №1 химический диктант.
2. Ответ по схеме “Опорный сигнал”. На данной схеме найти уравнения реакций, объясняющие амфотерные свойства алюминия, написать их в ОВР и указать окислитель, восстановитель. Приложение №1
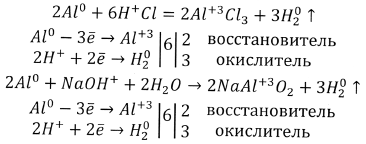
3. Ответ группы “Поиск”.
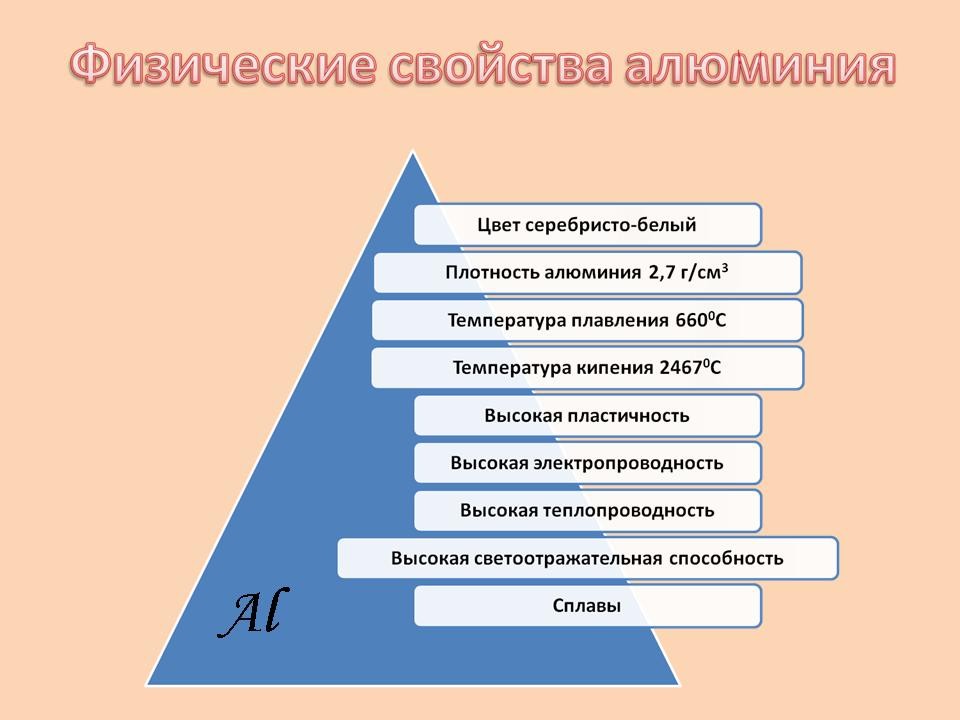
Каждый из учащихся, используя полученные физические и химические свойства, применение алюминия делает сообщение Приложение №3. Ответ группы “Экономист-расчетчик”.
Один из учащихся зачитывает задание, затем условие составленной задачи и объясняет ход решения, способ получения алюминия из данного сырья.
Задача должна иметь примерно такое содержание: “Сколько хлорида алюминия, содержащего 0,2 массовых долей примесей, необходимо взять для получения 30 кг алюминия?”.
Алюминий из хлорида алюминия можно получить электролизом расплава этого сырья, предварительно очистив его от примеси.
Дано: m (Al)=30кг
|
Решение.
|
m(AlCl3)чист |
4. Ответ группы “Экспериментатор”. Читают задание, называют схему превращений:
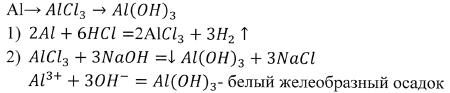
5.Отвечает ученик из класса (а ученик у доски, открыв её) проверяет правильность выполнения.
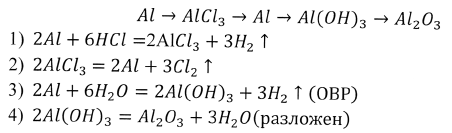
III. Объяснение нового материала. Итак, ребята, мы на этом уроке неоднократно встречались с формулами веществ, которые относятся к основным соединениям алюминия. Кто их назовёт? Ребята называют вещества, их формулы, а я записываю их на разных досках.
![]()
![]()
![]()
Al2O3
- оксид алюминия, химическая, молекулярная, эмпирическая формула. Al2O3 образован ионным видом связи.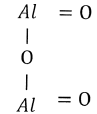
Al2O3
- твёрдое вещество, по твёрдости уступает только алмазу, тугоплавкое (2050°) В природе встречается в виде минерала-корунда, окрашенные кристаллы – это драгоценные камни: красные-рубины; синие – сапфиры; фиолетовые – аметисты.– амфотерный оксид, в воде не растворим и с ней не взаимодействует, но взаимодействует с кислотой и щёлочью.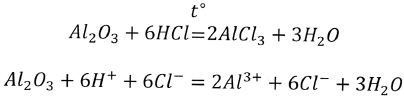
![]()
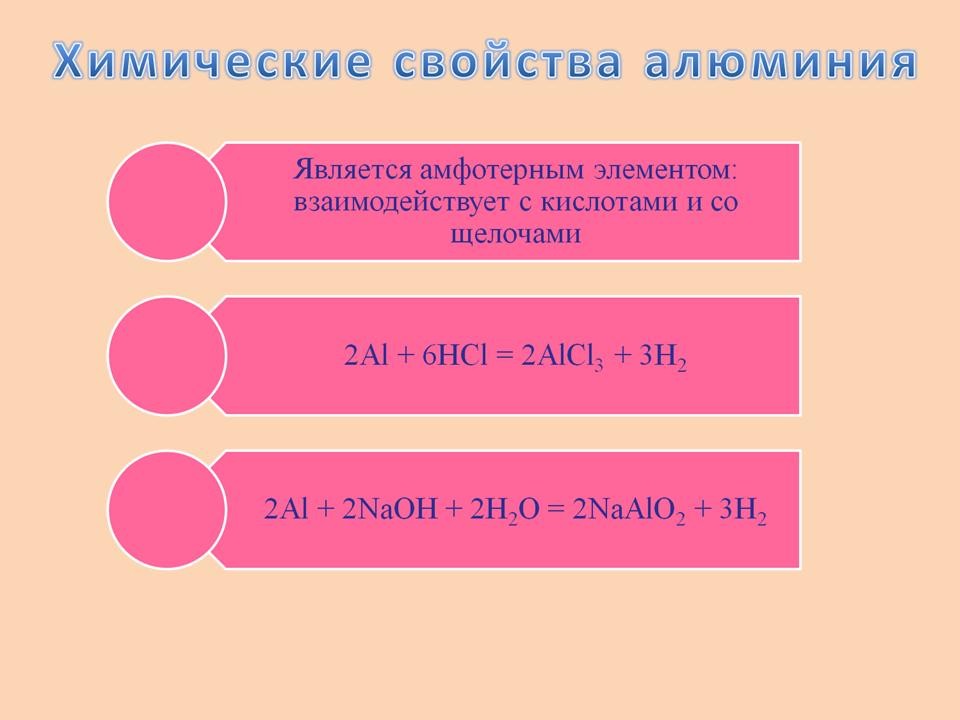
Взаимодействуя и с кислотой и со щёлочью, оксид алюминия проявляет амфотерные свойства.
Следующее соединение – гидроксид
алюминия ![]()
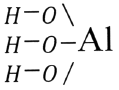 графическая формула.
графическая формула.
Это белое рыхлое вещество, в воде не растворимое. Для выяснения свойств данного вещества просмотрим кинофрагмент, в котором обратите внимание на получение гидроксида алюминия и его свойства, а затем проделаем лабораторный опыт. Записали в тетрадь и приготовились Приложение №2. Для слабых учащихся раздаю карточки: получение гидроксида алюминия и изучение его свойств.
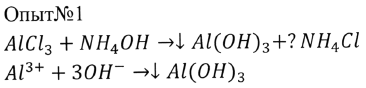
Вывод: как можно получить гидроксид алюминия
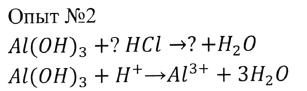
Вывод: какие свойства проявляет гидроксид алюминия в данной реакции?
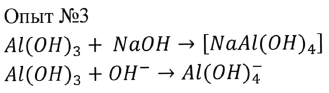
Вывод: какие свойства проявляет гидроксид алюминия в данной реакции?
Общий вывод: гидроксид алюминия-амфотерный оксид. За счёт чего образуется анион тетрагидроксидалюминат, если рассмотрим электронную схему образования гидроксида алюминия, она выглядит так:
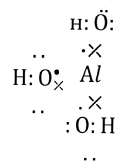
Из этой схемы видно, что у алюминия
всего три пары электронов. Три из них даёт
алюминий, а три атомы кислорода из гидроксогрупп.
А как вы знаете повышенной устойчивостью внешний
слой обладает когда на нём находится восемь
электронов, поэтому при взаимодействии со
щелочами гидроксид ион с тремя неподеленными
парами переходит к алюминию и за счёт (какого
вида связи?) донорно-акцепторного вида связи
образуется заряженный ион ![]() –
тетрагидроксоалюминат.
–
тетрагидроксоалюминат.
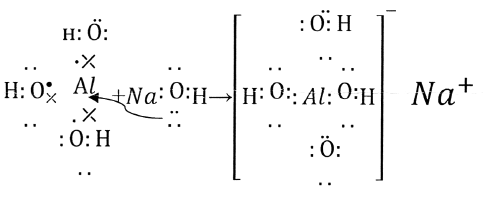
OH-
– ион гидроксогруппы – донор, атом алюминия – акцептор. Так образуются алюминаты при взаимодействии со щелочами.Соли алюминия– ![]() растворимы в воде, обладают
свойствами всех солей:
растворимы в воде, обладают
свойствами всех солей:
А) взаимодействуют с кислотами;
Б) взаимодействуют со щелочами;
В) взаимодействуют с растворами других солей;
Г) подвергаются гидролизу, среда всегда кислая.
Почему?
Уравнения реакций написать дома.
IV. Закрепление и задание на дом:
Используя уравнения реакций, написанные на
доске ещё раз закрепить, что все соединения
алюминия (![]() ;
; ![]() )
– амфотерные соединения.
)
– амфотерные соединения.
Домашнее задание.
Группе “Поиск” задание: выяснить состав алюмосиликата, применяемого на стекольном заводе, на котором мы были на экскурсии, а группе
“Экономист-расчетчик” составить задачу и на одном из уроков предложить классу.