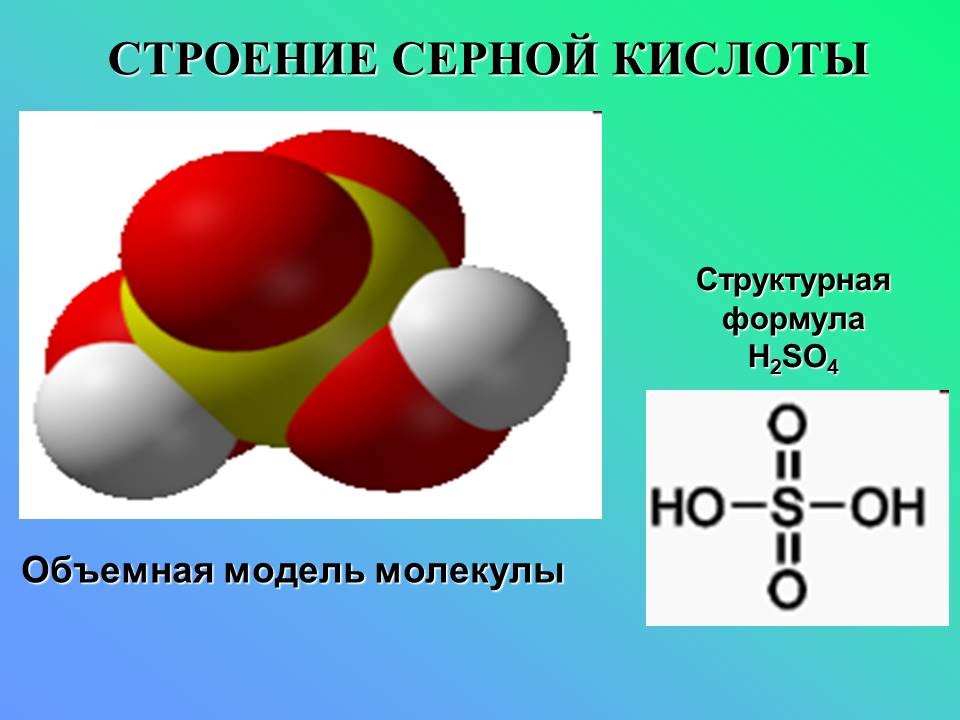
Кислоты — сложные вещества, состоящие из атома водорода, способного замещаться на атомы Ме, и кислотного остатка.
Кислоты - это электролиты, которые при диссоциации поставляют в водный раствор катионы водорода и никаких других положительных ионов не образуют:
H2SO4 = 2H+ + SO42−,
HF ↔ H+ + F−
Классификация
1) по силе
Сильные кислоты HCl, HBr, HI, HClO4, H2SO4, H2SeO4, HNO3, HMnO4, H2Cr2O7 и т.п.
Слабые кислоты HF, HCN, HClO, HNO2, H3PO4, CH3COOH, H2CO3, H2S, H4SiO4 и другие
2) по числу Н:
ОДНОосновные |
ДВУХосновные |
ТРЕХосновные |
HCl, HBr, |
H2S |
|
HNO3, HNO2 |
H2CO3 |
H3PO4 |
3) По кислотному остатку
БЕЗкислородные |
Кислородсодержащие (кислотные гидроксиды) |
HCl, HBr, H2S |
H2SO4, H2SeO4, HNO3 |
Способы получения кислот
| Кислородсодержащие | 1. Кислотный оксид+вода |
SO3+H2O= H2SO4 |
2. Неметалл+сильный окислитель |
P+5HNO3+ 2H2O = 3H3PO4+5NO |
|
3. Cоль+менее летучая кислота |
NaNO3+H2SO4= HNO3+NaHSO4 |
|
Бескислородные |
1. Водород+неметалл |
H2+Cl2= 2HCl |
2. Cоль+менее летучая кислота |
NaCl+H2SO4= 2HCl + NaHSO4 |
Химические свойства
| |
Бескислородные |
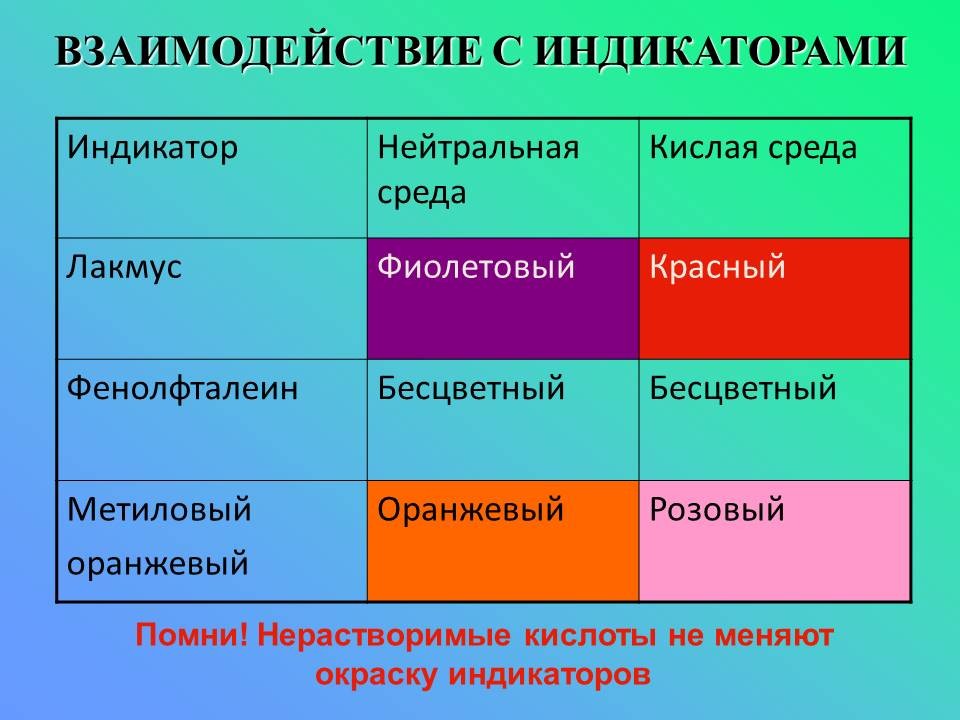
1. Изменяют окраску индикаторов: лакмус-красный, метилоранж-красный (только для растворимых кислот) |
|
2. Взаимодействие с металлами, стоящими до водорода |
|
H2SO4+Ca=CaSO4+H2 |
2HCl+Ca=CaCl2+H2 |
3. Взаимодействие с основными оксидами |
|
H2SO4 + CaO=CaSO4 + H2O |
2HCl+CaO=CaCl2 + H2O |
4.Взаимодействие с основаниями – реакция нейтрализации |
|
H2SO4+Ca(OH)2= CaSO4+2H2O |
2HCl+Ca(OH)2 = CaCl2+2H2O |
5. Взаимодействие с амфотерными оксидами |
|
H2SO4+ZnO=ZnSO4+H2O |
2HCl+ZnO = ZnCl2+H2O |
6. Взаимодействие с солями, если образуется малорастворимое, летучее или малодиссоциирующее вещество |
|
H2SO4+BaCl2=BaSO4+2HCl |
2HCl+Na2CO3 = 2NaCl+H2O+CO2 |
7. При нагревании |
|
Слабые кислоты легко разлагаются |
H2S=H2+S |
Взаимодействие серной (концентрированной) и азотной кислот с Ме:
Ме + кислота → соль + вода + ТРЕТИЙ продукт
Взаимодействие концентрированных серной и азотной кислот с Неме (S, P, Si, C):
Неме + кислота → Кислота Неме или оксид Неме + продукт восстановления кислот
Для:
H2SO4 (конц.) – SO2
HNO3(конц.) - NO2
Взаимодействие концентрированных серной и азотной кислот с бромидами, иодидами, сульфидами: (схемы реакций)
KI + H2SO4 (конц.) → H2S + I2 + K2SO4 +H2O
NaBr+ H2SO4 (конц.) → SO2 + Br2 + Na2SO4 +H2O
K2S + HNO3 (конц.) → NO2 + K2SO4 +H2O