Цель урока: Получение общей информации о карбоновых кислотах в процессе самостоятельной работы с опорой на применение ранее полученных знаний в комплексе новых ситуаций. На основании знаний электронного строения спиртов и альдегидов дать представление об электронном строении и взаимном влиянии функциональных групп в молекулах карбоновых кислот.
Тип урока: урок-исследование (урок ознакомления с новым материалом)
Задачи урока:
Образовательные
- Актуализировать знания учащихся по основным положениям теории органических веществ А.М.Бутлерова.
- Способствовать закреплению умений решать задачи на вывод формулы органического вещества.
- Совершенствовать исследовательские компетенции – разработка плана действий, формулировки гипотезы, определение методов исследования и презентация результатов.
Развивающие
- Развивать творческую активность и самостоятельность учеников.
- Способствовать продолжению развития устойчивого интереса к химической науке и практике.
- Развивать умения выделять главное, существенное.
- Продолжить формирование навыков безопасной работы с реактивами, выполнения химических опытов и умений работать в темпе, экономя время урока.
Воспитательные
- Способствовать формированию дисциплинированности, ответственного отношения к учебному труду.
- Формировать у каждого учащегося умения работать коллективом. При выполнении исследовательской работы считаться с мнением всей группы и корректно отстаивать свое.
Оборудование: компьютеры, видеопроектор, экран, видеофрагменты, презентации, шаростержневые модели, инструктивные карточки, необходимое лабораторное оборудование и реактивы (уксусная и соляная кислоты, лакмус, магний и цинк).
План урока
- Постановка цели урока и мотивация учебной деятельности учащихся.
- Актуализация субъективного опыта учащихся.
- Исследовательская работа.
а) по нахождению формулы неизвестного вещества;
б) по доказательству отношения вещества к определенному классу органических веществ, его строения и предсказания его возможных свойств;
в) экспериментальное подтверждение отношения неизвестного вещества к классу карбоновых кислот. - Контроль знаний.
- Подведение итогов урока.
- Домашнее задание.
Творческая группа, в составе 4 учащихся, под руководством учителя химии, возглавляющего НХОУ «Молекула», провела следующую предварительную работу:
- создание презентаций со звуковым сопровождением и анимацией;
- отснятие видеофрагментов химических опытов;
- изготовление шаростержневых моделей этанола, фенола, этаналя и этановой кислоты;
- фотографии;
Класс разделен на 3 группы, в каждую из которой входят по одному члену НХОУ, «Теоретики», «Исследователи» и «Практики».
Эпиграф. «Всякое вещество – от самого простого до самого сложного – имеет три различные, но взаимосвязанные стороны – свойство, состав, строение»
(В.М.Кедров).
Ход урока
1. Организационный этап. Мотивация.
Ребята, в связи с тем, что проводится урок-исследование, тема урока будет сформулирована после доказательства состава и свойств неизвестного вещества.
В школьной химической лаборатории, в шкафу, на одной из полок, был обнаружен пузырёк без подписи с неизвестным реактивом. В целях экономии реактивов лаборант решила определить, что это за вещество.
Цель нашего урока: исследовать строение и свойства неизвестного соединения, его отношение к одному из классов органических веществ.
2. Актуализация субъективного опыта учащихся.
Интеллектуальная разминка
Учитель: Кем и когда были сформулированы основные положения теории химического строения органических соединений? Ученик: Основные положения теориисформулированы А.М.Бутлеровым в 1861 г. (Приложение 1)
Учитель: Валентность углерода в органических соединениях может быть II и IV.
Ученик: Валентность углерода – чаще всего IV. (Приложение 2)
Учитель: Атомы, образующие молекулы органических веществ, связаны беспорядочно, без учета валентности.
Ученик: Атомы в молекулах связаны в определенной последовательности согласно их валентности.
Учитель: О какой зависимости ведется речь в одном из положений теории?
Ученик: Бутлеров в теории химического строения утверждал, что свойства органических соединений определяются составом и строением их молекул.
Учитель: Что является главной идеей теории химического строения?
Ученик: Химическое строение отражает зависимость свойств веществ от порядка соединения атомов и их взаимодействия.
Учитель: На основании основных положений теории А.М.Бутлерова нам предстоит провести исследование найденного лаборантом реактива.
3. Исследовательская работа.
(применение усвоенной системы знаний для объяснения новых фактов).
Группа «Теоретики» займется исследованием по определению искомой формулы вещества, группа «Исследователи» - должна доказать отношение вещества к определенному классу органических веществ, его строение и предсказать его возможные свойства, а группа «Практики» - экспериментальным путем исследовать и доказать предполагаемые свойства.
а) по нахождению формулы неизвестного вещества
Чтобы определить формулу неизвестного вещества, лаборант сожгла его, собрала и определила массы, качественный и количественный состав полученных продуктов. Задача группы: определить формулу вещества.
Отчет группы «Теоретики» по определению формулы вещества в форме презентации. (Приложение 3)
б) по доказательству отношения вещества к определенному классу органических веществ, его строения и предсказания его возможных свойств
Учитель: Предыдущей группой была определена молекулярная формула вещества. Теперь обращаемся к вам «Исследователи». Ваши предположения, что это за вещество? Каково его строение? Какими свойствами оно должно обладать? (Приложение 4)
Ученик: Я думаю, что это вещество должно входить в группу кислородосодержаших соединений.
Ученик: Предлагаю составить его структурную формулу. Составить ее можно на основании положений теории Бутлерова.
Учитель: Какие вы знаете классы, в составе которых имеется кислород? Чем характерны эти классы?
Ученик: К классам кислородосодержаших соединений, с которыми мы уже знакомы, относятся: предельные одноатомные спирты, многоатомные спирты, фенолы, альдегиды и кетоны. Их особенность состоит в том, что они содержат функциональные группы - гидроксильную и карбонильную. (Приложение 5)
Дальнейшее обсуждение учащимися группы, соотнесения найденной молекулярной формулы вещества к изученным классам кислородосодержаших соединений, приводит к тому, что попытки составить структурную формулу, не дали положительного результата.
Ученик: А что, если в состав этого вещества входят одновременно две функциональных группы?
Учащиеся составляют структурную формулу, которая принимает следующий вид:
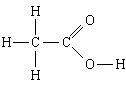
Ученик: Однозначно. Это вещество относится к ранее не изученному классу.
Учитель: Рассмотрите строение молекулы этого вещества. Из каких двух самостоятельных групп состоит его функциональная группа?
Ученик: Карбонильной: - С = О и Гидроксильной: - ОН
Учитель: Ребята, давайте предположим, какими свойствами может обладать это вещество. Для этого вам нужно вспомнить о взаимном влиянии атомов в молекуле. В чем заключается сущность взаимного влияния атомов?
Ученик: Взаимное влияние состоит во взаимодействии электронных структур атомов, что приводит к смещению электронной плотности химических связей.
Учитель: Предлагаю мысленно «расчленить» неизвестную функциональную группу на две: гидроксильную и карбонильную – и вспомнить, какое влияние они оказывают на молекулу в отдельности.
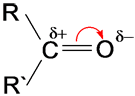
Ученик: Связь в карбонильной группе С=О полярная, плотность смещена к атому кислорода. (Приложение 6 – 1 слайд)
Ученик: Из электронной формулы спиртов видно, что кислород в молекуле имеет две неподеленные электронные пары. (Приложение 6 – 2 слайд)
![]()
Кислород в гидроксильной группе, обладая значительной электроотрицательностью, оттягивает электронную плотность связи O—Н в свою сторону. По этой причине наблюдается подвижность атома водорода в гидроксильной группе спирта
Учитель: Какие свойства придает спиртам наличие гидроксильной группы?
Ученик: За счет подвижности атома водорода спирты проявляют слабые кислотные свойства.
Учитель: И вот две эти функциональные группы соединены между собой.
Как распределена электронная плотность в получившемся фрагменте? Как это отражается на свойствах данного класса? (Приложение 6 – 3 слайд)
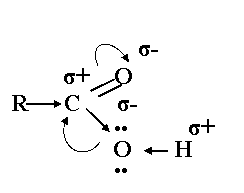
Ученик: Гидроксильная группа связана с углеводородным радикалом, и с карбонильной группой. В этом случае более электроотрицательный карбонильный кислород будет оттягивать на себя ![]() - электроны двойной связи. Атом углерода карбонильной группы приобретает некоторый положительный заряд. В результате этого атом углерода притягивает к себе электронное облако от атома кислорода гидроксильной группы. Компенсируя смещенную электронную плотность, атом кислорода гидроксильной группы оттягивает к себе электронное облако соседнего атома водорода. Вследствие этого связь между атомами кислорода и водорода в гидроксильной группе становится более полярной и атом водорода приобретает большую подвижность, чем в спиртах – происходит отрыв атома водорода в гидроксильной группе
- электроны двойной связи. Атом углерода карбонильной группы приобретает некоторый положительный заряд. В результате этого атом углерода притягивает к себе электронное облако от атома кислорода гидроксильной группы. Компенсируя смещенную электронную плотность, атом кислорода гидроксильной группы оттягивает к себе электронное облако соседнего атома водорода. Вследствие этого связь между атомами кислорода и водорода в гидроксильной группе становится более полярной и атом водорода приобретает большую подвижность, чем в спиртах – происходит отрыв атома водорода в гидроксильной группе

Ученик: Из курса неорганической химии мы знаем, вещества, которые в растворах диссоциируют с образованием катионов водорода, называются кислотами. Поэтому можно смело утверждать, что неизвестным веществом является органическая кислота.
в) экспериментальное подтверждение отношения неизвестного вещества к классу карбоновых кислот
Группа «Практики» экспериментальным путем исследует предполагаемые свойства органической кислоты в сравнении с неорганическими кислотами. Экспериментальное исследование проводится по инструктивной карточке. (Приложение 7)
Отчет группы проходит с просмотром видеофрагментов.
Вывод. Химические свойства зависят от взаимного влияния атомов. Водород карбоксильной группы обладает повышенной подвижностью, и кислоты в водном растворе диссоциируют с отщеплением иона водорода и изменяют окраску индикаторов.
Учитель: Ребята, настал момент, когда мы можем сформулировать тему урока. Мне только осталось записать ее на доске. «Одноосновные карбоновые кислоты. Строение и свойства».
Далее учитель знакомит учащихся с изомерией и номенклатурой карбоновых кислот, закрепляет знания об образовании водородных связей и их решающем значении для физических свойств веществ.
4. Контроль знаний.
Проводится компьютерное тестирование.
5. Подведение итогов урока.
Учитель: Ребята, давайте подведем итог нашего урока. Достигнута ли цель урока? Что нового вы узнали на уроке?
Ученик: В ходе исследования мы определили, что на полке лабораторного шкафа хранилась уксусная кислота.
Ученик: Определили молекулярный состав класса карбоновых кислот, выяснили, что в молекуле уксусной кислоты ![]() имеется реакционно-способная группа, которая определяет химические свойства вещества. Что, взаимное влияние атомов в молекуле приводит к подвижности атома водорода в -ОН группе и проявлению кислотных свойств.
имеется реакционно-способная группа, которая определяет химические свойства вещества. Что, взаимное влияние атомов в молекуле приводит к подвижности атома водорода в -ОН группе и проявлению кислотных свойств.
Учитель: Что вам понравилось на уроке?
Ученик: Мне понравилось…
Ученик: Мне было интересно так как…
6. Домашнее задание.
Обязательный уровень: §20 упр.6,9. Стр. 175 - 189
Творческое задание: в форме презентации придумать не менее 3 тестов по изученной теме.
Повышенный уровень: сравнить силу кислот (этановой, пропановой, бутановой).